题目内容
【题目】一定温度下,在三个体积均为 2.0L 的恒容密闭容器中发生如下反应:A(g)![]() B(g)+C(g)
B(g)+C(g) ![]() H>0。
H>0。
起始物质的量(mol) | 平衡物质的量(mol) | |||||
容器 | 温度(℃) | A(g) | B(g) | C(g) | 达到平衡所需时间(s) | |
Ⅰ | T1 | 0.20 | 0.10 | 0.10 | t1 | |
Ⅱ | T2 | 0.40 | t2 | |||
Ⅲ | T3 | 0.20 | 0.15 | 0.15 | t3 | |
下列说法正确的是( )
A.达到平衡的时间:t3>t1
B.反应达到平衡时,A 的转化率:容器Ⅱ>容器
C.反应达到平衡时,容器 I 中的平均速率为 v(A)=(0.10/t1)mol/(L·s)
D.T1 时,该反应的平衡常数为 0.05
【答案】D
【解析】
A.I与III相比,起始量相同,III中反应正向进行程度大,可知T3>T1,升高温度反应速率加快,则达到平衡的时间:t3<t1,故A错误;
B.I与II的温度不同、起始量不同,温度、压强均影响平衡移动,且温度未知,不能比较A的转化率,故B错误;
C.反应达到平衡时,容器I中的平均速率为v(A)=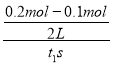 =
=![]() mol/(L·s),故C错误;
mol/(L·s),故C错误;
D.T1时,结合表中数据可知,
A(g)![]() B(g)+C(g)
B(g)+C(g)
开始/mol 0.2 0 0
转化/mol 0.1 0.1 0.1
平衡/mol 0.1 0.1 0.1
浓度/mol/L 0.05 0.05 0.05
T1时,该反应的平衡常数为K=![]() mol·L-1=0.05mol·L-1,故D正确;
mol·L-1=0.05mol·L-1,故D正确;
故选D。

练习册系列答案
相关题目
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D