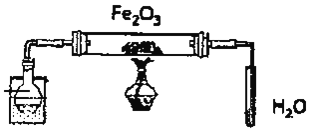题目内容
【题目】某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
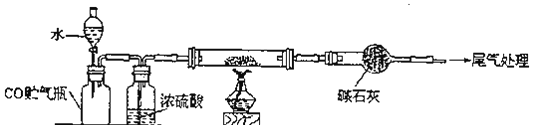
(1)乙同学认为甲同学的结论是错误的,他的理由是__________________________(用化学方程式表示),所以他认为应该检验__________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。

(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)_______。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸; ④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用____________________________________。
(4)C装置中出现的现象是_______________________________________________,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式___________________________。
【答案】4HNO3![]() 4NO2↑+O2↑+2H2O CO2 ④ 常温下存在平衡体系:2NO2
4NO2↑+O2↑+2H2O CO2 ④ 常温下存在平衡体系:2NO2![]() N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。 C中溶液变浑浊(或产生白色沉淀) 4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O
N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。 C中溶液变浑浊(或产生白色沉淀) 4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O
【解析】
(1)浓硝酸受热易分解产生二氧化氮气体,4HNO3![]() 4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
(2)只要存在浓硝酸被加热的情况都有可能产生二氧化氮气体,不能证明是C与浓硝酸发生了反应,所以最合理的操作是④;
(3)常温下存在平衡体系:2NO2![]() N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
(4)若C与浓硝酸反应则有二氧化碳生成,与氢氧化钡溶液反应生成白色沉淀;C的溶液中还含有少量氮元素,只以NO3-形式存在,说明混合气体中仍有NO2,与氢氧化钡溶液、氧气反应生成硝酸钡溶液,化学方程式为4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O。

【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A.升温不利于正反应生成Ni(CO)4(g)
B.在25 ℃时,反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正>v逆
D.在80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
【题目】有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阳离子和一种阴离子且互不重复)。
阳离子 | K+、Na+、Ba2+、NH |
阴离子 | CH3COO-、Cl-、OH-、SO |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的电离程度相同;D物质的焰色反应呈黄色;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成有刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是_______B的化学式_______
(2)写出C溶液和D溶液反应的化学方程式___________
(3)25 ℃时,pH=9的A溶液和pH=9的C溶液中水的电离程度小的是___(填A或C)。
(4) A溶液的pH大于7,用离子方程式表示原因______。