��Ŀ����
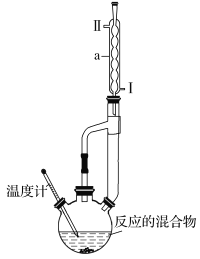
����Ŀ����������һ����ɫҺ�壬ijʵ��С��������ͼ��ʾ��װ���Ʊ������͡���ѧ��Ӧԭ����ʵ��װ��������ʾ��
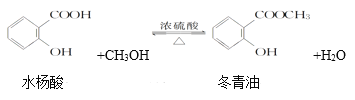
������й����������ʾ��
��Է������� | �ܶ�/g��cm��3 | �е�/�� | �ܽ��� | |
������ | 152 | 1.180 | 222.2 | ����ˮ |
ʵ�鲽��������ʾ��
��������ƿ�м���6.9g(0.05mol)ˮ�����24g(0.75mol)�״�����С�ĵؼ���6mLŨ���ᣬҡ�ȡ�
�ڼ���2����ʯ(�����Ƭ)��װ������a����ʯ�����ϱ����¶���85��95�棬����1.5h��
�۷�Ӧ��ϣ�����ƿ��ȴ������50mL����ˮ��Ȼ��ת������Һ©������ȥˮ�㣬���л����ٵ����Һ©���У�������50mL5%̼��������Һ��30 mLˮϴ�ӡ�
�ܽ����������������ƿ�У�����0.5g��ˮ�Ȼ��ơ�
����ֲ�Ʒ���������ռ�221��224�����֣�������Ϊ6.8g��
��ش��������⣺
��1����ʵ����Ũ�����������___��
��2��װ��������a��������___����ˮ��Ϊ___(����������������)���¶ȼƵ����˹��Ϊ___(�����)��
��50�� ��100�� ��300��
��3����̼��������Һϴ�ӵ�Ŀ����___����ˮϴ��ʱ����Ʒ��___(����������������)�㡣
��4��������ˮ�Ȼ��Ƶ�Ŀ����____��
��5������ʵ���ж����͵IJ���Ϊ___��
���𰸡���������ˮ�� ���������� I �� ��ȥ�ֲ�Ʒ��δ��Ӧ��ˮ��������� �²� ���մֲ�Ʒ�е�ˮ�֣���������ʱˮ�ֽ����Ʒ�� 89.5%
��������
(1)��ʵ��ķ�Ӧԭ����������Ӧ��Ũ������������Ӧ�Ĵ�����ͬʱ������Ũ�����������ɵ�ˮ���ٽ�ƽ�������ƶ�����߲��ʡ�
(2)����a�����������ܣ�ˮ���¿����룬�Ͽ����������������������Ч������ˮ��Ϊ��ʵ���¶ȿ�����85��95�棬Ӧѡ������Ϊ100����¶ȼƣ�ѡ�ڡ�
(3)��̼��������Һϴ�ӳ�ȥ�ֲ�Ʒ��δ��Ӧ��ˮ��������ᡣ�����ܶȵ�����֪�����͵��ܶȴ���ˮ���ܶȣ��ʲ�Ʒ���²㣬ˮ��Һ���ϲ㡣
(4)����ˮ�Ȼ������մֲ�Ʒ�е�ˮ�֣���������ʱˮ�ֽ����Ʒ�С�
(5)�����ϼ״�������ʹˮ������ȫ��Ӧ������ˮ������������Ͽ����ɶ�����0.05mol��m��0.05mol��152g��mol��1��7.6g�������͵�ʵ�����Ϊ![]() ��100%��89.5%��
��100%��89.5%��




