题目内容
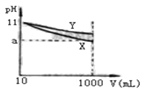
【题目】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:在容器为1L的密闭容器中充入1molCO2和3molH2 ,平衡时CO2的物质的量为0.25mol,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量______(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:__________。甲醇分子中的化学键类型是________(填“离子键”或“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是__________,发生的是__________(填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:___________________
(5)平衡时H2的转化率为__________平衡时混合气体中CH3OH(g)的体积分数为__________。
(6)下列事实能表明该反应已达平衡状态的是(_______)(填序号)
A.CO2(g)的浓度不再发生变化
B.单位时间内消耗1mol CO2的同时生成3mol H2
C.在一个绝热的容器中,混合物的温度不再发生变化
D.在一个容积固定的容器内,压强不再发生变化
【答案】小于 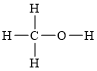 共价键 甲醇(或CH3OH) 氧化 升高温度、增大反应物浓度、增大压强等 75% 30% ABCD
共价键 甲醇(或CH3OH) 氧化 升高温度、增大反应物浓度、增大压强等 75% 30% ABCD
【解析】
(1)由图像可知,该反应中反应物总能量高于生成物总能量,因此属于放热反应,反应过程中,断裂反应物中的化学键吸收的总能量小于形成生成物中的化学键释放的总能量;
(2)乙醇结构式为: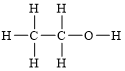 ,甲醇与乙醇结构类似,均属于醇类,因此甲醇的结构式为:
,甲醇与乙醇结构类似,均属于醇类,因此甲醇的结构式为: ;甲醇属于分子化合物,分子中化学键均属于共价键;
;甲醇属于分子化合物,分子中化学键均属于共价键;
(3)甲醇燃料电池以KOH溶液为电解质,负极上甲醇发生氧化反应生成Na2CO3,电极反应式为:![]() ;
;
(4)升高温度、增大反应物浓度、增大压强等均能增大合成甲醇的化学反应速率;
(5)平衡时CO2的物质的量为0.25mol,根据化学计量数可知,平衡时H2的物质的量为[3-(1-0.25)×3]mol=0.75mol,则H2的转化率为![]() ;由化学计量数以及CO2转化量可知,平衡时CH3OH(g)、H2O(g)的物质的量为0.75mol,则平衡时混合气体中CH3OH(g)的体积分数为
;由化学计量数以及CO2转化量可知,平衡时CH3OH(g)、H2O(g)的物质的量为0.75mol,则平衡时混合气体中CH3OH(g)的体积分数为![]() ;
;
(6)A.CO2(g)的浓度不再发生变化,可说明正逆反应速率相等,即反应已达平衡状态,故A符合题意;
B.根据化学计量数可知,单位时间内消耗1mol CO2的同时会消耗3mol H2,若同时生成3mol H2,则说明正逆反应速率相等,即反应已达平衡状态,故B符合题意;
C.该反应正向为放热反应,在一个绝热的容器中,混合物的温度不再发生变化,说明正逆反应速率相等,即该反应达到平衡状态,故C符合题意;
D.该反应正向为气体物质的量减小的反应,在恒容容器中,气体压强之比等于气体总物质的量之比,当容器内压强不再变化,说明气体的物质的量不再变化,可说明反应已达到平衡状态,故D符合题意;
故答案为:ABCD。

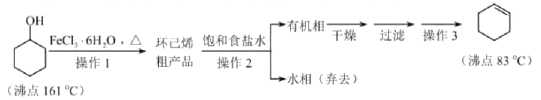
【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
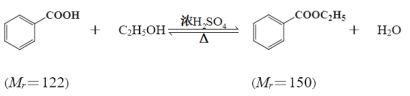
已知:
颜色、状态 | 沸点(℃) | 密度(g·cm-3) | |
苯甲酸 | 无色、片状晶体 | 249 | 1.265 9 |
苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 |
乙醇 | 无色澄清液体 | 78.3 | 0.789 3 |
环己烷 | 无色澄清液体 | 80.8 | 0.731 8 |
*苯甲酸在100 ℃会迅速升华。
实验步骤如下:
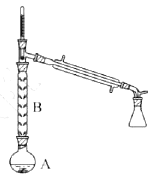
a.在100 mL圆底烧瓶中加入12.20 g苯甲酸、25 mL乙醇(过量)、20 mL 环己烷,以及4 mL浓硫酸,混合均匀并加入沸石,按下图所示装好仪器,控制温度在65~70 ℃加热回流2 h。反应时环己烷—乙醇—水会形成“共沸物”(沸点62.6 ℃)蒸馏出来,再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
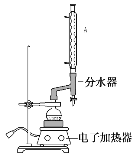
b.反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
c.将烧瓶内反应液倒入盛有适量水的烧杯中,加入饱和Na2CO3溶液。
d.用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213 ℃的馏分。
e.检验合格,测得产品体积为12.86 mL。
回答下列问题:
(1)反应中浓硫酸的作用是:________________。步骤a中加入沸石作用:____________。温度在65~70 ℃加热的方法是:________________。
(2)仪器A的名称是:________________。该反应类型为______________。
(3)关于步骤d中的分液操作叙述正确的是________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞。将分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗下口的玻璃活塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,需将玻璃塞上的凹槽对准漏斗口上的小孔
(4)上述实验中饱和碳酸钠溶液的作用是___________________。
(5)当达到该反应的限度,也即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的有(填序号)_______________________。
①单位时间里,生成1mol苯甲酸乙酯,同时生成1mol水
②单位时间里,生成1mol苯甲酸乙酯,同时生成1mol乙醇
③单位时间里,消耗1mol乙醇,同时消耗1mol苯甲酸
④正反应的速率与逆反应的速率相等
⑤合物中各物质的浓度不再变化
⑥混合物中各物质的浓度相等