题目内容
【题目】Ⅰ.纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:____________。
(2)实验室中用过氧化氢制取氧气的化学方程式为_______________,当生成标准状况下2.24L O2时,转移电子为______ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:______。(只写第一步)
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:___________
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
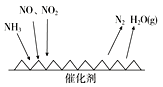
(1)由上图可知SCR技术中的氧化剂为________。
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________________________________
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
反应②:CH3OCH3(g)+H2O(g)![]() 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol
反应③:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=___________kJ/mol。
CH3OCH3(g)+3H2O(g) △H3=___________kJ/mol。
【答案】![]() 2H2O2
2H2O2![]() 2H2O+O2↑ 0.2 H2O2
2H2O+O2↑ 0.2 H2O2![]() H++HO2- 向褪色后的溶液中加入NaOH溶液,若变红,甲的说法正确;若不变红,乙的说法正确 NO、NO2 2NH3+NO+NO2
H++HO2- 向褪色后的溶液中加入NaOH溶液,若变红,甲的说法正确;若不变红,乙的说法正确 NO、NO2 2NH3+NO+NO2![]() 2N2+3H2O -122.6
2N2+3H2O -122.6
【解析】
(1)过氧化氢的电子式为: ![]() ;
;
(2)过氧化氢在二氧化锰做催化剂的条件下反应生成水和氧气,方程式为: 2H2O2![]() 2H2O+O2↑ ;当生成2.24L O2时,即生成0.1mol氧气,转移0.2mol电子;
2H2O+O2↑ ;当生成2.24L O2时,即生成0.1mol氧气,转移0.2mol电子;
(3) H2O2为二元弱酸,其酸性比碳酸弱,所以电离方程式用可逆符号,电离方程式为H2O2![]() H++HO2-;
H++HO2-;
(4)向褪色后的溶液中加入氢氧化钠溶液,若变红,说明原溶液中没有氢氧根离子,甲的说法正确;若不变红,说明乙的说法正确;
Ⅱ.(1)从图分析,一氧化氮和二氧化氮中的氮元素化合价降低,做氧化剂;
(2) 用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1.,反应生成氮气和水,结合电子守恒和质量守恒得方程式为:2NH3+NO+NO2![]() 2N2+3H2O;
2N2+3H2O;
Ⅲ.根据盖斯定律分析,反应①:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1= -49.6kJ/mol;反应②:CH3OCH3(g)+H2O(g)
CH3OH(g)+H2O(g) △H1= -49.6kJ/mol;反应②:CH3OCH3(g)+H2O(g)![]() 2CH3OH(g) △H2= +23.4kJ/mol;有①×2-②得反应③:2CO2(g)+6H2(g)
2CH3OH(g) △H2= +23.4kJ/mol;有①×2-②得反应③:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3= -49.6×2-23.4= -122.6kJ/mol。
CH3OCH3(g)+3H2O(g) △H3= -49.6×2-23.4= -122.6kJ/mol。