题目内容
【题目】关于化合物![]() 说法错误的是( )
说法错误的是( )
A. 1mol该化合在一定条件下加氢最多可消耗5mol H2
B. 该化合物最多有15个原子共面
C. 该化合物是乙炔的同系物
D. 该化合物与![]() 互为同分异构体
互为同分异构体
【答案】C
【解析】A项,化合物![]() 分子中含有一个苯环和一个碳碳叁键,所以1mol该化合在一定条件下加氢最多可消耗5mol H2,故A正确;B项,该有机物分子中共有17个原子,甲基中有两个氢原子一定不在苯环所在的平面上,所以该化合物最多有15个原子共面,故B正确;C项,同系物应为同类物质且组成相差一个或多个“-CH2-”,乙炔(C2H2)与该化合物(C9H8)不符合同系物概念,故C错误;D项,该化合物(C9H8)与
分子中含有一个苯环和一个碳碳叁键,所以1mol该化合在一定条件下加氢最多可消耗5mol H2,故A正确;B项,该有机物分子中共有17个原子,甲基中有两个氢原子一定不在苯环所在的平面上,所以该化合物最多有15个原子共面,故B正确;C项,同系物应为同类物质且组成相差一个或多个“-CH2-”,乙炔(C2H2)与该化合物(C9H8)不符合同系物概念,故C错误;D项,该化合物(C9H8)与![]() (C9H8)分子式相同而结构不同,互为同分异构体,故D正确。
(C9H8)分子式相同而结构不同,互为同分异构体,故D正确。

【题目】现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
元素 | 性质 |
A | 一种核素的原子核内不含中子 |
B | 原子核外电子有6种不同运动状态 |
C | 最高价氧化物的水化物与其氢化物可生成盐 |
D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
F | 该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
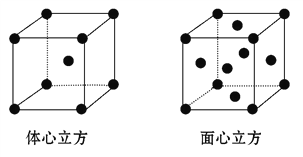
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。