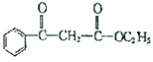
题目内容
【题目】关于如图所示的原电池,下列说法正确的是( )

A. 电子从锌电极通过导线流向铜电极,再流回锌电极,形成闭合电路
B. 盐桥中的阳离子向硫酸铜溶液中迁移
C. 锌电极发生还原反应
D. 铜电极上发生的电极反应为2H++2e-===H2↑
【答案】B
【解析】该原电池中,Zn易失电子作负极、Cu作正极,正极电极反应式为Cu2++2e-=Cu,负极电极反应式为Zn-2e-=Zn2+,电子从负极沿导线流向正极,盐桥中阳离子向正极移动、阴离子向负极移动,据此分析解答。
A.锌作负极、铜作正极,电子从锌电极通过导线流向铜电极,溶液中阳离子移向正极,阴离子移向负极,形成闭合回路,故A错误;
B.Zn易失电子作负极、Cu作正极,阳离子向正极移动,则盐桥中阳离子向硫酸铜溶液迁移,故B正确;
C.锌失电子发生氧化反应,铜电极上铜离子得电子发生还原反应,故C错误;
D.铜电极上铜离子得电子发生还原反应,电极反应式为Cu2++2e-=Cu,故D错误。
故B正确。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】亚硝酸钠(化学式为 NaNO2)是一种常用的防腐剂,回答下列问题:
(1)NaNO2 中 N 元素的化合价为_________.
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式_________________。
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠______千克。
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为________(填化学式)。
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为____________。
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.70 | 20.02 | 20.00 | 19.98 |
该样品中亚硝酸钠的质量分数为_________.(已知:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O)