题目内容
【题目】精炼铜工业中阳极泥的综合利用具有重要意义。一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:
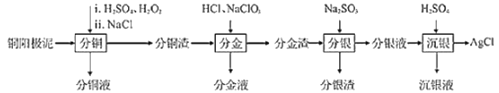
已知:ⅰ.分金液中含金离子主要成分为[AuCl4]-;分金渣的主要成分为AgCl;
ⅱ.分银液中含银离子主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-
ⅲ.“分铜”时各元素的浸出率如表所示。

(1)由表中数据可知,Ni的金属性比Cu______。分铜渣中银元素的存在形式为(用化学用语表示)______。
(2)“分金”时,单质金发生反应的离子方程式为______。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。
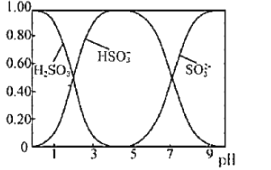
“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgCl的原因为______。调节溶液的pH不能过低,理由为______(用离子方程式表示)。
(4)工业上,用镍为阳极,电解0.1mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:
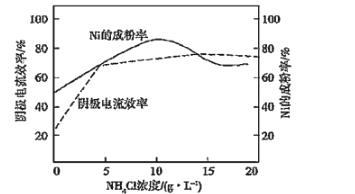
为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为______g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为______。
【答案】强 AgCl 2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl 避免产生污染气体SO2 10 H2
【解析】
由流程可知,铜阳极泥加入硫酸、过氧化氢和氯化钠分铜,“分铜”时,单质铜发生反应是铜在酸性溶液中被过氧化氢氧化生成硫酸铜和水,“分铜”时加人足量的NaCl的主要作用为使溶解出的Ag+形成AgCl进入分铜渣,加入盐酸和氯酸钠分金,分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,分金渣加入亚硫酸钠过滤得到分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-加入硫酸沉银,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl,以此解答该题。
(1)由表中数据可知,Ni的浸出率大,则Ni的金属性比Cu强,分铜渣中银元素的存在形式为AgCl;
故答案为:强;AgCl;
(2)分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,反应的离子方程式为2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O;
故答案为:2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O;
(3)分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-,H2SO4电离出的H+降低了SO32-的浓度,平衡正向进行,能够析出AgCl的原因为:H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl,调节溶液的pH不能过低理由为:避免产生污染气体SO2;
故答案为:H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl;避免产生污染气体SO2;
(4)根据图2可知,NH4Cl的浓度为10g![]() L-1时,镍的成粉率最高,所以NH4Cl的浓度最好控制为10g
L-1时,镍的成粉率最高,所以NH4Cl的浓度最好控制为10g![]() L-1,当NH4Cl浓度大于15g
L-1,当NH4Cl浓度大于15g![]() L-1时,阴极有气体生成,阴极发生还原反应,溶液中铵根离子水解溶液呈酸性,阴极电极反应式为2H++2e-=H2↑或2NH4++2H2O+2e-=2NH3
L-1时,阴极有气体生成,阴极发生还原反应,溶液中铵根离子水解溶液呈酸性,阴极电极反应式为2H++2e-=H2↑或2NH4++2H2O+2e-=2NH3![]() H2O+H2↑,阴极生成的气体为H2;
H2O+H2↑,阴极生成的气体为H2;
故答案为:10;H2。