题目内容
【题目】(1)下列几组物质中,互为同位素的有__________,互为同素异形体的有__________,互为同系物的有__________,互为同分异构体的有__________,属于同种物质的__________。
①O2和O3 ②35Cl和37Cl③CH3CH3和CH3CH2CH3④CH3CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3
⑤H2、D2和T2⑥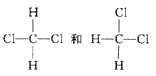 ⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
(2)含有10个及10个以下碳原子的烷烃,其一氯代物只有一种的共有4种,请写出这4种烷烃的结构简式和名称:_______、_______、______、______。
【答案】② ① ③④ ⑦ ⑥⑧ 甲烷,CH4 乙烷,CH3CH3 新戊烷,C(CH3)4 2,2,3,3-四甲基丁烷,(CH3)3CC(CH3)3
【解析】
(1)质子数相同而中子数不同的同一种元素的不同核素互为同位素。由同一种元素形成的不同单质,互称为同素异形体。分子式相同而结构不同的化合物互为同分异构体。结构相似,分子组成相差若干个CH2原子团的同一类物质互为同系物。性质和结构都完全相同的属于同一种物质;
(2)烷烃的一氯代物只有一种,说明分子中只有一类氢原子,据此解答。
(1)①O2和O3均是氧元素形成的单质,互为同素异形体;
②35Cl和37Cl的质子数相同,中子数不同,互为同位素;
③CH3CH3和CH3CH2CH3均是烷烃,分子组成相差1个CH2原子团,互为同系物;
④CH3CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3均是烷烃,分子组成相差1个CH2原子团,互为同系物;
⑤H2、D2和T2均表示氢气分子;
⑥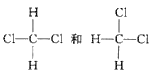 的结构和性质完全相同,是同一种物质;
的结构和性质完全相同,是同一种物质;
⑦CH3(CH2)2CH3和(CH3)2CHCH3的分子式均是C4H10,结构不同,互为同分异构体;
⑧CH3CH(CH3)CH3和CH(CH3)3的结构和性质完全相同,是同一种物质;
因此互为同位素的有②,互为同素异形体的有①,互为同系物的有③④,互为同分异构体的有⑦,属于同种物质的是⑥⑧;
(2)含有10个及10个以下碳原子的烷烃,其一氯代物只有一种,说明分子中氢原子均只有一类,则符合条件的共有4种,分别是甲烷,结构简式为CH4,乙烷,结构简式为CH3CH3,新戊烷,结构简式为C(CH3)4,2,2,3,3-四甲基丁烷,结构简式为(CH3)3CC(CH3)3。

【题目】已知部分弱酸的电离常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(25 ℃) | Ka=1.8×10-5 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
请回答下列问题:
(1)25 ℃时,在某二元酸 H2A 溶液中存在的所有微粒为:H+、OH-、HA-、A2-、H2O,写出 H2A 的 电离方程式_____。
(2)25 ℃时,在 0.5 mol·L-1 的醋酸溶液中由醋酸电离出的[H+]约是_________,是该溶液 中由水电离出的[H+]的_____倍,醋酸的电离度为_____(填百分数)
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:______________________________。
(4)25 ℃时,CH3COOH 与 CH3COONa 的混合溶液,若测得混合液 pH=6,则溶液中[CH3COO-]-[Na+]=_____(填准确数值)。
(5)25 ℃时,将 a mol·L-1 的醋酸与 b mol·L-1 氢氧化钠溶液等体积混合,反应后溶液恰好显中性, 用 a、b 表示醋酸的电离常数为_____。