题目内容
下列反应的离子方程式书写正确的是
| A.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:Ba2+ + 2OH- + NH4+ + H+ + SO42- = BaSO4↓+ NH3·H2O + H2O |
| B.碳酸钙溶于醋酸:CaCO3 + 2H+ =Ca2+ + CO2↑+ H2O |
| C.向硅酸钠溶液中通入过量的CO2:SiO32-+ CO2 + H2O= H2SiO3↓+ CO32- |
| D.澄清石灰水与过量小苏打溶液混合:Ca2+ + OH- + HCO3-="=" CaCO3↓+H2O |
A
解析试题分析:A、刚好沉淀完全,NH4HSO4与Ba(OH)2物质的量之比为1:1,离子方程式为:Ba2+ + 2OH- + NH4+ + H+ + SO42- = BaSO4↓+ NH3·H2O + H2O,正确;B、醋酸为弱酸,应用CH3COOH表示,错误;C、CO2过量,应生成HCO3?,错误;D、过量小苏打使Ca(OH)2中OH?完全反应:Ca2+ + 2OH- + 2HCO3-="=" CaCO3↓+2H2O+CO32?,错误。
考点:本题考查离子方程式的书写。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
下列离子方程式不正确的是
A.用铜电极电解NaCl溶液:2 Cl-+2H2O  Cl2↑+H2↑+2 OH- Cl2↑+H2↑+2 OH- |
| B.氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| C.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO |
| D.Cl2通入FeBr2溶液中,Cl2与FeBr2物质的量之比4︰5:10Fe2++6Br-+8Cl2=10Fe3++3Br2+16Cl- |
下列各组离子中,一定能在指定溶液中大量共存的是:
| A.澄清透明的无色溶液:ClO-、CrO42-、Al3+、SO42- |
| B.能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- |
| C.常温呈中性的溶液中:Fe3+、K+、Cl-、SO42- |
| D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |
溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是( )
| A.d点溶液中含有的溶质只有Na2SO4 |
| B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓, Mg2++2OH-= Mg(OH)2↓ |
| C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+ |
| D.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
将由NaOH、BaCl2、Al2(SO))3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断不正确的是( )
| A.AB段发生反应的离子方程式为:Ba2++SO42-=BaSO4↓ |
| B.E点对应横坐标稀硫酸的体积为70 ml |
| C.D点表示的沉淀的化学式为Al(OH)3、BaSO4 |
| D.E点沉淀比A点沉淀质量大2.33g |
某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是
| A.Mg2+、Ba2+、Br- | B.Al3+、CH3COO-、Cl- |
| C.Mg2+、Cl-、Fe2+ | D.Na+、NH4+、Cl- |
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
| A.等体积、等物质的量浓度的明矾溶液和Ba(OH)2溶液混合:3Ba2++6OH -+2Al3++3SO42- ="==" 2Al(OH)3↓+3BaSO4↓ |
| B.FeSO4酸性溶液暴露在空气中:4Fe2+ + O2 + 2H2O = 4Fe3+ + 4OH - |
| C.向AlCl3 溶液中投入过量Na:2Al 3+ + 6Na + 6H2O = 2Al(OH)3 ↓ + 6Na+ + 3H2↑ |
| D.向FeBr2溶液中通入少量Cl2:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2 Br2 + 6Cl- |
水溶液X中只可能溶有K+、Mg2+、Al3+、[Al(OH)4]-、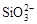 、
、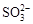 、
、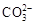 、
、 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验: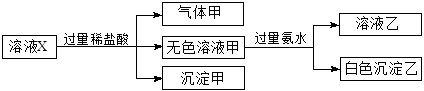
下列判断正确的是( )
| A.气体甲一定是纯净物 |
B.K+、[Al(OH)4]-和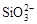 一定存在于溶液X中 一定存在于溶液X中 |
| C.沉淀甲是硅酸和硅酸镁的混合物 |
D.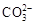 和 和 一定不存在于溶液X中 一定不存在于溶液X中 |
 mol/L,一定会发生反应的离子组是
mol/L,一定会发生反应的离子组是