题目内容
利用海水资源进行化工生产的部分工艺流程如图: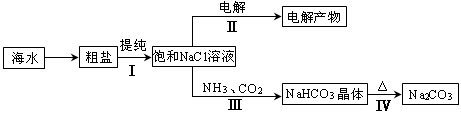
(1)流程I中,欲除去粗盐中含有的Ca2+、Mg2+、SO42-等离子,需将粗盐溶解后,按序加入药品进行沉淀、过滤等。加入药品和操作的顺序可以是 。
a.Na2CO3、NaOH、BaCl2、过滤、盐酸 b.NaOH、BaCl2、Na2CO3、过滤、盐酸
c.NaOH、Na2CO3、BaCl2、过滤、盐酸 d.BaCl2、Na2CO3、NaOH、过滤、盐酸
(2)流程II中,电解饱和NaCl溶液的离子方程式为 。通电开始后,阳极区产生的气体是 ,阴极附近溶液pH会 (填“增大”、“减小”或“不变”)。
(3)流程III中,通过反应得到NaHCO3晶体。下图为NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲线,其中能表示NaHCO3溶解度曲线的是 ,化学反应方程式是 。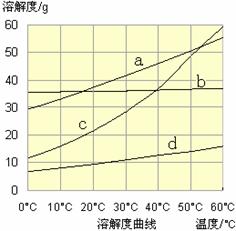
(4)流程IV中,所得纯碱常含有少量可溶性杂质,提纯它的过程如下:将碳酸钠样品加适量水溶解、 、 、过滤、洗涤2-3次,得到纯净Na2CO3?10H2O,Na2CO3?10H2O脱水得到无水碳酸钠,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2=" +473.63" kJ·mol-1
把该过程产生的气态水完全液化释放的热能全部用于生产Na2CO3所需的能耗(不考虑能量损失),若生产1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = 。
(16分)
(1)bd(3分,只选b或d得1分,全对得3分,凡其它有错答案不得分)。
(2) 2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分,写“通电”不扣分、漏反应条件、无“↑”、未配平只扣1分); Cl2(或氯气)(1分),增大(1分)
2OH-+H2↑+Cl2↑(2分,写“通电”不扣分、漏反应条件、无“↑”、未配平只扣1分); Cl2(或氯气)(1分),增大(1分)
(3)d (2分) NaCl + CO2 + NH3 + H2O="=" NaHCO3↓+ NH4Cl(2分,未写“↓”扣1分)
(4)蒸发浓缩 冷却结晶(2分) — 44.00 kJ/mol(3分,无单位扣1分,没有符号“-”的不得分)
解析试题分析:(1)a项,虽然能除去杂质及过量碳酸钠和氢氧化钠,但是过量氯化钡没有除去,故a选项错误;b项,既能除去杂质及过量的氢氧化钠、氯化钡、碳酸钠,又不引入新的杂质,故b选项正确;c项,虽然能除去杂质及过量的氢氧化钠、碳酸钠,但是过量的氯化钡没有除去,故c选项错误;d项,既能除去杂质及过量的氯化钡、碳酸钠、氢氧化钠,又不引入新的杂质,故d选项正确;(2)用惰性电解饱和食盐水可以制备氢氧化钠、氢气、氯气,该反应实质为2Cl-+2H2O 2OH-+H2↑+Cl2↑;阴离子移向阳极,氯离子比氢氧根离子容易失去电子,发生氧化反应,产生黄绿色的气体,即氯气;阳离子移向阴极,氢离子比钠离子容易得到电子,发生还原反应,则阴极产生无色气体,即氢气,由于氢离子被消耗,则阴极附近氢离子浓度减小,所以阴极附近溶液的pH增大;(3)流程III的反应属于复分解反应,即NaCl+NH3+CO2+H2O==NaHCO3↓+NH4Cl(或者NH3+H2O==NH3?H2O、NH3?H2O+CO2==NH4HCO3、NH4HCO3+NaCl="=" NaHCO3↓+NH4Cl),该反应能够发生的原因是NH4HCO3、NaCl的溶解度均大于NaHCO3,则图中溶解度最小的d表示NaHCO3;(4)由于被提纯物和杂质都是可溶物,杂质可能是NaCl等,根据混合物分离提纯的方法推断,应选择结晶法分离出碳酸钠晶体,因此需要将碳酸钠样品加适量水溶解、蒸发浓缩、冷却结晶或降温结晶、过滤、洗涤,得到纯净的Na2CO3?10H2O,Na2CO3?10H2O脱水得到无水碳酸钠;先将已知两个热化学方程式编号为①②,观察发现①+②可得③Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(g) ΔH3=" +532.36" kJ·mol-1,依题意可知④Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(l) ΔH4=" +92.36" kJ·mol-1,观察发现(④—③)/10可以得到:H2O(g)="=" H2O(l) ΔH=(ΔH4—ΔH3)/10=" —44" kJ·mol-1。
2OH-+H2↑+Cl2↑;阴离子移向阳极,氯离子比氢氧根离子容易失去电子,发生氧化反应,产生黄绿色的气体,即氯气;阳离子移向阴极,氢离子比钠离子容易得到电子,发生还原反应,则阴极产生无色气体,即氢气,由于氢离子被消耗,则阴极附近氢离子浓度减小,所以阴极附近溶液的pH增大;(3)流程III的反应属于复分解反应,即NaCl+NH3+CO2+H2O==NaHCO3↓+NH4Cl(或者NH3+H2O==NH3?H2O、NH3?H2O+CO2==NH4HCO3、NH4HCO3+NaCl="=" NaHCO3↓+NH4Cl),该反应能够发生的原因是NH4HCO3、NaCl的溶解度均大于NaHCO3,则图中溶解度最小的d表示NaHCO3;(4)由于被提纯物和杂质都是可溶物,杂质可能是NaCl等,根据混合物分离提纯的方法推断,应选择结晶法分离出碳酸钠晶体,因此需要将碳酸钠样品加适量水溶解、蒸发浓缩、冷却结晶或降温结晶、过滤、洗涤,得到纯净的Na2CO3?10H2O,Na2CO3?10H2O脱水得到无水碳酸钠;先将已知两个热化学方程式编号为①②,观察发现①+②可得③Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(g) ΔH3=" +532.36" kJ·mol-1,依题意可知④Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(l) ΔH4=" +92.36" kJ·mol-1,观察发现(④—③)/10可以得到:H2O(g)="=" H2O(l) ΔH=(ΔH4—ΔH3)/10=" —44" kJ·mol-1。
考点:考查物质制备化学工艺流程,涉及粗盐的分离和提纯、电解饱和食盐水的原理、电极产物及电极附近溶液pH的变化、溶解度曲线在水溶液里复分解反应中的应用、化学方程式、盖斯定律、热化学方程式的书写等。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛。铁还有很多重要的化合物及其化学反应。如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反应的平衡常数表达式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
则△H=_______。
(3)在t0C时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| | Fe | H2O(g) | Fe3O4 | H2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
①甲容器中H2O的平衡转化率为_______ (结果保留一位小数)。
②下列说法正确的是_______ (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
| | Fe | H2O(g) | Fe3O4 | H2 |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
| | Fe | H2O(g) | Fe3O4 | H2 |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1 | 4 |
| C/mol | m | n | p | q |
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是
________(用A、B、C表示)。
(5)已知Fe(OH)3的Ksp=2.79×10-39,而FeCl3溶液总是显示较强的酸性,若某FeCl3溶液的pH为3,则该溶液中c(Fe3+)=________mol ? L-1 (结果保留3位有效数字)
常温下钛的化学活性很小,在较高温度下可与多种物质反应。
(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下: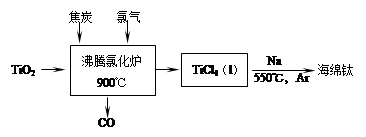
① 沸腾氯化炉中发生的主要反应为: 。
②已知:Ti(s) +2Cl2(g)=TiCl4(l) ΔH=a kJ·mol-1;
2Na(s) +Cl2(g)=2NaCl(s) ΔH=b kJ·mol-1;
Na(s)=Na(l) ΔH=c kJ·mol-1;
则TiCl4(l) +4Na(l)=Ti(s) +4NaCl(s) ΔH= kJ·mol-1。
③ TiCl4遇水强烈水解,写出其水解的化学方程式 。
(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示,二氧化钛电极连接电 极,该极电极反应为: 。但此法会产生有毒气体,为减少对环境的污染,在电池中加入固体氧离子隔膜(氧离子能顺利通过),将两极产物隔开,再将石墨改为金属陶瓷电极,并通入一种还原性气体,该气体是 。
(3)海绵钛可用碘提纯,原理为: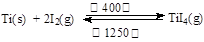 ,下列说法正确的是 。
,下列说法正确的是 。
| A.该反应正反应的ΔH>0 |
| B.在不同温度区域,TiI4的量保持不变 |
| C.在提纯过程中,I2 的作用是将粗钛从低温区转移到高温区 |
| D.在提纯过程中,I2 可循环利用 |
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol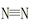 键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为 kJ。
键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为 kJ。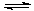 H++ SO42-
H++ SO42-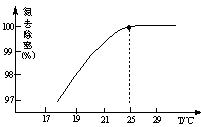



 )。
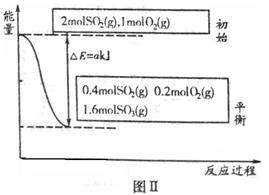
)。 2SO3(g) ?H=-196.6 kJ·mol-1
2SO3(g) ?H=-196.6 kJ·mol-1 2NO2(g) ?H=-113.0 kJ·mol-1
2NO2(g) ?H=-113.0 kJ·mol-1