题目内容
碳铵是一种较常使用的化肥,它在常温下易分解.某化学兴趣小组对碳铵的成分存在疑问,进行了如下探究.
【定性试验】检验溶液中的阴、阳离子.
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成.再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色.
(1)根据实验现象,推测碳铵中所含有阴离子可能是 和 .
(2)根据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是 .
【定量试验】测定碳铵中C元素和N元素质量比.该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如图所示.

(1)碳铵固体应放在 中进行加热.
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(2)从安全的角度考虑,尾气处理的装置可以选用 .
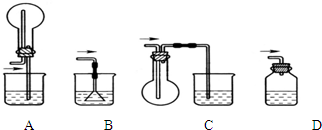
(3)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg.由此测得N元素的质量是 g.
(4)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量.请你评价该方案是否合理. (填“合理”“不合理”),理由是 .
【定性试验】检验溶液中的阴、阳离子.
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成.再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色.
(1)根据实验现象,推测碳铵中所含有阴离子可能是
(2)根据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是
【定量试验】测定碳铵中C元素和N元素质量比.该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如图所示.

(1)碳铵固体应放在
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(2)从安全的角度考虑,尾气处理的装置可以选用

(3)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg.由此测得N元素的质量是
(4)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量.请你评价该方案是否合理.
考点:性质实验方案的设计,铵盐,实验装置综合
专题:实验设计题
分析:【定性试验】取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成,白色沉淀为碳酸钙;再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色,则气体为氨气;
【定量试验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,
(1)因加热装置后连接U形管,以此选择仪器;
(2)尾气处理,应防止倒吸;
(3)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g;
(4)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,若混有碳酸氢根离子或测量不准确,则不合理;若碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量,则合理,以此来解答.
【定量试验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,
(1)因加热装置后连接U形管,以此选择仪器;
(2)尾气处理,应防止倒吸;
(3)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g;
(4)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,若混有碳酸氢根离子或测量不准确,则不合理;若碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量,则合理,以此来解答.
解答:
解:【定性实验】取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成,白色沉淀为碳酸钙,盐中阴离子可能HCO3-、CO32-;再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色,则气体为氨气,则原固体中含铵根离子,
(1)由上述分析可知,阴离子可能为HCO3-、CO32-,故答案为:HCO3-;CO32-;
(2)碳铵与足量NaOH溶液加热反应的离子方程式可能是NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O),
故答案为:NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O);
【定量实验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,
(1)因加热装置后连接U形管,则选择仪器只能为试管,故答案为:A;
(2)尾气处理,应防止倒吸,B不能防止倒吸,C中气体收集时导管应短进,D中为密闭容器可能会炸裂,只有A装置收集及防倒吸,故答案为:A;
(3)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g,则含N质量为
(a-b)g,故答案为:
(a-b);
(4)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,则
①不合理,因为碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确;
②合理,因为碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量;
③不合理;测得的结果不准确,
故答案为:不合理;碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确.
(1)由上述分析可知,阴离子可能为HCO3-、CO32-,故答案为:HCO3-;CO32-;
(2)碳铵与足量NaOH溶液加热反应的离子方程式可能是NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O),
故答案为:NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O);
【定量实验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,
(1)因加热装置后连接U形管,则选择仪器只能为试管,故答案为:A;
(2)尾气处理,应防止倒吸,B不能防止倒吸,C中气体收集时导管应短进,D中为密闭容器可能会炸裂,只有A装置收集及防倒吸,故答案为:A;
(3)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g,则含N质量为
| 14 |
| 17 |
| 14 |
| 17 |
(4)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,则
①不合理,因为碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确;
②合理,因为碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量;
③不合理;测得的结果不准确,
故答案为:不合理;碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确.
点评:本题考查性质实验方案的设计,综合性较强,侧重分析与实验能力的综合考查,注意实验装置的作用,尤其注意(4)小题属于开放性试题,回答“合理”或“不合理”且理由能做出相应解释均可,有利于学生发散思维能力的训练,题目难度中等.

练习册系列答案
相关题目
下列有关溶液中离子浓度的关系,不正确的是( )
| A、NaHC03溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B、常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C、0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D、相同温度下,0.2mol/L的CH3COOH溶液中c(H+)小于0.1mol/L的CH3COOH中c(H+)的两倍 |
金属M和N可构成如图所示的装置.下列分析正确的是( )
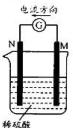

| A、金属活性性N>M |
| B、M逐渐溶解 |
| C、负极反应为2H++2e-═H2↑ |
| D、SO42-向M极定向移动 |
下列说法正确的是( )
| A、常温下,等物质的量浓度的三种溶液①(NH4)2CO3②NH4Cl③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
| B、等物质的量浓度的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C、常温下,在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、AlO2-、SO32-等离子不可能大量共存 |
| D、一定温度下,将盐酸滴加入醋酸钠溶液中至呈中性.此时溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
下列离子反应方程式中,属于水解反应的是( )
| A、CN-+H2O?HCN+OH- |
| B、NH3?H2O?NH4++OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、H2CO3?HCO3-+H+ |
下列说法正确的是( )
| A、检验碘乙烷中的碘元素,先在NaOH水溶液中加热后滴入硝酸银溶液 |
| B、分子式为C3H6的物质只有一种 |
| C、用新制Cu(OH)2悬浊液可以鉴别乙酸、葡萄糖、淀粉三种溶液 |
| D、油脂、蛋白质和纤维素均属于高分子化合物 |
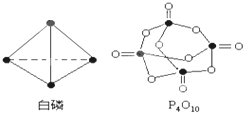 白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子.如图:
白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子.如图: