题目内容
7.进行如下实验:在A锥形瓶中放入绿豆粒大的碳酸钙,在B锥形瓶中放入5g粉末状的碳酸钙,分别加入50mL 1mol•L-1盐酸.如图中(图中:x表示时间;y表示锥形瓶中碳酸钙减小的质量),能正确表示实验结果的是( )| A. | 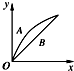 | B. | 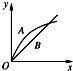 | C. | 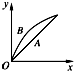 | D. |  |
分析 增大固体的接触面积可以加快化学反应速率,根据盐酸和碳酸钙的反应情况来确定消耗的碳酸钙的量的多少,以此解答该题.
解答 解:发生CaCO3+2HCl=CaCl2+H2O+CO2↑,n(CaCO3)=0.05mol,n(HCl)=0.05L×1mol/L=0.05mol,由方程式可知盐酸不足,则生成的二氧化碳的体积相同,因碳酸钙粉末与盐酸的反应速率比碳酸钙固体的反应速率要快,则只有C正确.
故选C.
点评 本题考查外界条件对反应速率的影响为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意影响化学反应速率的因素以及物质发生变化的实质.

练习册系列答案
相关题目
15.红磷与氯气反应时,当生成PCl3和PCl5的物质的量之比为2:1时,参加反应的红磷与氯气的物质的量之比为(提示:2P+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2PCl3 2P+5Cl2$\frac{\underline{\;点燃\;}}{\;}$2PCl5)( )
| A. | 6:11 | B. | 2:3 | C. | 2:5 | D. | 6:5 |
2.往纯水中加入下列物质,能使水的电离平衡发生移动的是( )
| A. | NaCl | B. | NaOH | C. | 酒精 | D. | CH3COOH |
19.阿伏加德罗常数约为6.02×1023mol-1.下列叙述中正确的是( )
| A. | 标准状况下,2.24L苯中约含有3.612×1023个碳原子 | |
| B. | 常温常压下,氧气和臭氧的混合物16g中约含有6.02×1023个氧原子 | |
| C. | 1L 1mol/L醋酸溶液中离子总数为1.204×l024 | |
| D. | 0.5mol CH4中约含有3.01×1023个电子 |
16.用氯气消毒过的自来水配制下列溶液时,会使所配的溶液的溶质发生变化的是( )
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤KI.
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤KI.
| A. | 只有①② | B. | 只有①④⑤ | C. | 只有②④⑤ | D. | ①②③④⑤ |
 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1