题目内容
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
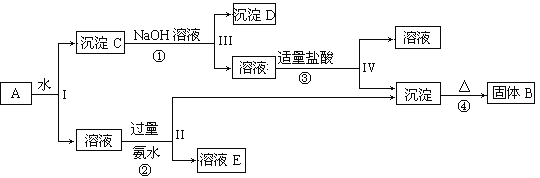
据此回答下列问题:
(1)I、II、III、IV四步中分离溶液和沉淀所采取的操作名称是____________。
(2)①、③反应的离子方程式:
①_____________________________________________________________;
③_____________________________________________________________。
(3)有人认为③用盐酸不是太好,改为通入足量的一种气体,这种气体为______。该离子反应方程式为:________。
【答案】过滤 Al2O3+2OH-=AlO2-+H2O AlO2-+H++H2O=Al(OH) 3↓ CO2 AlO2- +CO2+2H2O=Al(OH) 3↓+HCO3-
【解析】
根据氧化铝、氧化铁的性质分析;根据离子反应条件分析;
由流程可知,Al2O3和Fe2O3不溶于水,则沉淀C为Al2O3和Fe2O3,氧化铁与碱不反应,则沉淀D为Fe2O3,反应②③中生成的沉淀为Al(OH)3,受热分解生成B为Al2O3,反应②为KAl(SO4)2和氨水的反应,则溶液E为K2SO4、(NH4)2SO4、NH3.H2O,
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离方法为过滤,故答案为:过滤;
(2)由上述分析可知,B为Al2O3,则反应①为Al2O3+2OH-=2AlO2-+H2O,反应③为AlO2-+H++H2O=Al(OH)3↓;
(3)反应③中使用盐酸的量不容易被控制,易过量,是生成的氢氧化铝溶解,所以可以向偏铝酸钠溶液中通入CO2气体,离子方程式为:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-。

【题目】以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
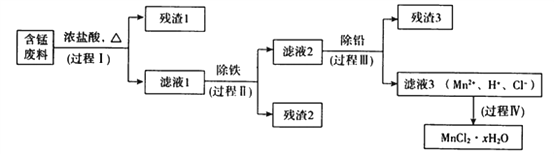
资料a.Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b.生成氢氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
注:金属离子的起始浓度为0.1 mol·L-1
(1)过程Ⅰ的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnOOH与浓盐酸反应的离子方程式是_______________________________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:_________________________________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a.2Fe2++Cl2=2Fe3+2Cl-
b.4Fe2++O2+4H+=2Fe3++2H2O
c.……
写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法,
ⅰ.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ⅱ.焙烧法:将滤液1浓缩得到的固体于290℃焙烧,冷却,取焙烧物,加水溶解,过滤,再加盐酸酸化至pH小于5.5。
已知:焙烧中发生的主要反应为2FeCl3+3O2=2Fe2O3+3Cl2,MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在_____________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下,取m1g样品,置于氯化氢氛围中加热至失去全部结晶水时,质量变为m2g。则x=____________。