题目内容
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定。回答下列问题:
I.岩脑砂的制备
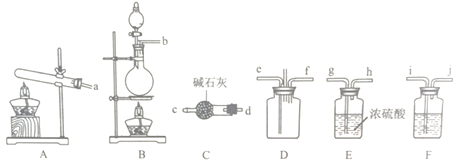
(1)该实验中用浓盐酸与二氧化锰反应制取所需氯气,写出该反应的化学反应方程式_____,装置F中的试剂是___________(填试剂名称)。
(2)为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:a→____→ef←___(用小写字母和箭头表示,箭头方向与气流方向一致)。
(3)装置D处有两个明显的不足之处,其中之一为:导管太细,生成的氯化按固体会堵塞导管,之二为:___________。
(4)证明氨气和氯气反应有岩脑砂生成,需要的检验试剂(试纸)中,除了蒸馏水、稀HNO3、NaOH溶液外,还需要______。热的浓氯化铵溶液可以清洗溶解铁器表面锈迹,写出相关反应的离子方程式_________________。
II.岩脑砂中元素的测定
准确称取ag岩脑砂,与足量的氧化铜混合加热(2NH4Cl+3CuO![]() 3Cu+N2↑+2HC1↑+3H2O),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
3Cu+N2↑+2HC1↑+3H2O),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
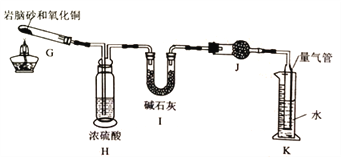
(5)设置装置H的目的是______________。
(6)若装置I增重bg,利用装置K洲得气体体积为VL(已知常温常压下气体摩尔体积为24.5L/mol),则岩脑砂中m(N):m(Cl)=_____(用含b、V的代数式表示,不必化简)。若测量体积时气体温度高于常温(其他操作均正确且忽略气体摩尔体积的改变),则m(N)比正常值______(填“偏高”、“偏低”或“无影响”)。
【答案】 MnO2+4HCl![]() MnCl2+Cl2↑+2H2O 饱和食盐水 →dc hg←ji←b 无尾气处理装置 AgNO3溶液、红色石蕊试纸(其他合理答案即可) 6NH4++Fe2O3
MnCl2+Cl2↑+2H2O 饱和食盐水 →dc hg←ji←b 无尾气处理装置 AgNO3溶液、红色石蕊试纸(其他合理答案即可) 6NH4++Fe2O3![]() 2Fe3++6NH3↑+3H2O 吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响 (28V/24.5):(35.5b/36.5) 偏高
2Fe3++6NH3↑+3H2O 吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响 (28V/24.5):(35.5b/36.5) 偏高
【解析】(1)该实验中用浓盐酸与二氧化锰反应制取氯气,同时生成氯化锰和水,反应的化学反应方程式为MnO2+4HCl![]() MnCl2+Cl2↑+2H2O,装置F是用于除去氯气中的氯化氢,所装的试剂是饱和食盐水;(2)为了使氨气和氯气在D中充分混合,左边A装置利用氯化铵和氢氧化钙加热制取氨气,利用装置C进行干燥后进入D混合,氨气密度比空气小由长导管进从而逆向混合;右边由装置B利用二氧化锰和浓盐酸加热反应制取氯气,再经装置F除去氯化氢,再经装置E干燥后进入装置D混合;故装置的合理连接顺序为:a→dc→ef←hg←ji←b ;(3)装置D处有两个明显的不足之处,其中之一为:导管太细,生成的氯化按固体会堵塞导管,之二为:无尾气处理装置,氨气与氯气直接排放到空气中会造成污染;(4)检验岩脑砂(主要成分为NH4Cl)可利用强碱加热产生能使湿润红色石蕊试纸变蓝检验铵根离子,利用硝酸和硝酸银检验氯离子,故试剂(试纸)中,除了蒸馏水、稀HNO3、NaOH溶液外,还需要AgNO3溶液、红色石蕊试纸;热的浓氯化铵溶液水解使溶液呈酸性,可以清洗溶解铁器表面锈迹,反应的离子方程式为6NH4++Fe2O3
MnCl2+Cl2↑+2H2O,装置F是用于除去氯气中的氯化氢,所装的试剂是饱和食盐水;(2)为了使氨气和氯气在D中充分混合,左边A装置利用氯化铵和氢氧化钙加热制取氨气,利用装置C进行干燥后进入D混合,氨气密度比空气小由长导管进从而逆向混合;右边由装置B利用二氧化锰和浓盐酸加热反应制取氯气,再经装置F除去氯化氢,再经装置E干燥后进入装置D混合;故装置的合理连接顺序为:a→dc→ef←hg←ji←b ;(3)装置D处有两个明显的不足之处,其中之一为:导管太细,生成的氯化按固体会堵塞导管,之二为:无尾气处理装置,氨气与氯气直接排放到空气中会造成污染;(4)检验岩脑砂(主要成分为NH4Cl)可利用强碱加热产生能使湿润红色石蕊试纸变蓝检验铵根离子,利用硝酸和硝酸银检验氯离子,故试剂(试纸)中,除了蒸馏水、稀HNO3、NaOH溶液外,还需要AgNO3溶液、红色石蕊试纸;热的浓氯化铵溶液水解使溶液呈酸性,可以清洗溶解铁器表面锈迹,反应的离子方程式为6NH4++Fe2O3![]() 2Fe3++6NH3↑+3H2O;(5)设置装置H的目的是吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响;(6)若装置I增重bg,则产物的氯化氢的物质的量为
2Fe3++6NH3↑+3H2O;(5)设置装置H的目的是吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响;(6)若装置I增重bg,则产物的氯化氢的物质的量为![]() ,利用装置K测得气体体积为VL(已知常温常压下气体摩尔体积为24.5L/mol),则氮气的物质的量为
,利用装置K测得气体体积为VL(已知常温常压下气体摩尔体积为24.5L/mol),则氮气的物质的量为![]() ,则岩脑砂中m(N):m(Cl)=
,则岩脑砂中m(N):m(Cl)=![]() ;若测量体积时气体温度高于常温,氮气体积偏大,则m(N)比正常值偏高。
;若测量体积时气体温度高于常温,氮气体积偏大,则m(N)比正常值偏高。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某研究小组为了探究NaClO溶液的性质,设计了下列实验,并记录实验现象。
实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
| ① | 0.2 mol/L NaClO溶液 | 饱和Ag2SO4溶液 | 产生白色沉淀 |
② | CH3COOH溶液 | 光照管壁有无色气泡 | ||
③ | 0.2mol/LFeSO4酸性溶液和KSCN溶液 | 溶液变红 | ||
④ | 0.2mol/L的AlCl3溶液 | 产生白色沉淀 |
则以下判断不正确的是
A. 实验①:发生的反应为Ag++ClO-+H2O=AgCl↓+2OH- B. 实验②:无色气体为O2
C. 实验③:还原性强弱顺序Fe2+>Cl- D. 实验④:ClO-与Al3+的水解相互促进