题目内容
右图是某条件下 与
与 反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是
反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是

 与
与 反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是
反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是
A.该反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g)ΔH=+92kJ/mol 2NH3(g)ΔH=+92kJ/mol |
B. 曲线是加入催化剂时的能量变化曲线 曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热数值会减小 |
D.反应2NH3(g)  N2(g)+3H2(g) ΔH=+92kJ/mol N2(g)+3H2(g) ΔH=+92kJ/mol |
D
试题分析:从图中可以看出,该反应的反应物总能量高于生成物的总能量,即为放热反应,A错D对;加入催化剂,反应的活化能降低,b曲线才是加入催化剂的能力变化曲线;反应热是反应前后能量之差,与反应历程无关,故催化剂的加入对反应热没有影响。
点评:反应热是历年高考的常考知识点,特别是反应历程的能量变化图,考生在备考过程中应把握图中的相关信息。

练习册系列答案
相关题目
 2NH3(g) △H=-93.0kJ /mol;另据报道,一定条件下:2N2(g)+6H2O(l)
2NH3(g) △H=-93.0kJ /mol;另据报道,一定条件下:2N2(g)+6H2O(l)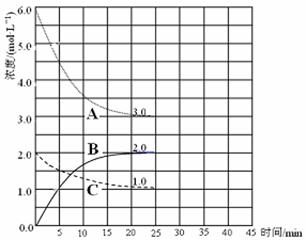
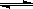 CH3OH(g);CO的转化率与温度、压强的关系如图所示。
CH3OH(g);CO的转化率与温度、压强的关系如图所示。
 Ag+(aq)+Cl-(aq)。25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号)。
Ag+(aq)+Cl-(aq)。25oC时,现将足量AgCl分别放入:①l00mL蒸馏水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化镁溶液;④100mL 0.1 mol?L-1氯化钠溶液。充分搅拌后,相同温度下Ag+浓度由大到小的顺序是 (填写序号)。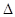 H=-67.7 kJ·mol-1
H=-67.7 kJ·mol-1 F-(aq)+H+(aq)
F-(aq)+H+(aq)  CH4(g)+O2(g)=
CH4(g)+O2(g)=