题目内容
9.下列物质中,属于纯净物的是( )| A. | 洁净的空气 | B. | 纯净的盐水 | C. | 石油 | D. | 冰水 |
分析 纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;纯净物为可以从以下理解:宏观:由一种物质组成的物质,微观:由同种分子构成,组成固定,有固定的物理性质和化学性质的物质,有专门的化学符号.据此结合常见物质的组成成分逐项分析即可.
解答 解:A.空气是多组分的混合气体,除氧、氮及稀有气体组分之外,还有二氧化碳和水蒸气等,洁净的空气属于混合物,故A错误;
B.纯净的盐水为盐和水形成的分散系,属于混合物,故B错误;
C.石油是多种烃的混合物,故C错误;
D.冰水混合物为水的固态、液态两种形式,是氢和氧元素组成的纯净物化合物,化学式为H2O,故D正确.
故选D.
点评 本题考查纯净物的判别,难度不大,注意把握纯净物概念,宏观:由一种物质组成的物质.微观:由同种分子构成.组成固定,有固定的物理性质和化学性质的物质,有专门的化学符号.

练习册系列答案
相关题目
3.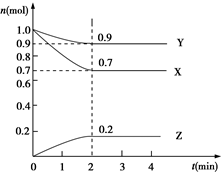 某温度时,在2L的密闭容器中,X、Y、Z三种物质(其中X为固体,Y、Z为气体)的物质的量随时间的变化曲线如图所示:
某温度时,在2L的密闭容器中,X、Y、Z三种物质(其中X为固体,Y、Z为气体)的物质的量随时间的变化曲线如图所示:
(1)由图中所给数据进行分析,该反应的化学方程式为X+3Y?2Z;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.05mol•(L•min)-1;
(3)若其它条件不变,只改变一个反应条件,将反应速率的变化填入表中空格里.
(填字母:A.增大 B.减小 C.不变)
 某温度时,在2L的密闭容器中,X、Y、Z三种物质(其中X为固体,Y、Z为气体)的物质的量随时间的变化曲线如图所示:
某温度时,在2L的密闭容器中,X、Y、Z三种物质(其中X为固体,Y、Z为气体)的物质的量随时间的变化曲线如图所示:(1)由图中所给数据进行分析,该反应的化学方程式为X+3Y?2Z;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.05mol•(L•min)-1;
(3)若其它条件不变,只改变一个反应条件,将反应速率的变化填入表中空格里.
(填字母:A.增大 B.减小 C.不变)
| 改变条件 | 降低温度 | 增加X的量 | 使用催化剂 | 容器体积减半 |
| 速率变化 |
4.25℃,pH=5的HCl和pH=9的NaOH溶液以体积比11:9混合,混合液的pH为( )
| A. | 7.2 | B. | 8 | C. | 6 | D. | 7 |
14.下列反应中生成物总能量低于反应物总能量的是( )
| A. | 氢气还原氧化铜 | B. | 高锰酸钾分解 | ||
| C. | 锌放入稀硫酸 | D. | 碳和水蒸气在高温下反应 |
1.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Ca2+、Fe2+、NO3-、CO32- | |
| B. | $\frac{K}{c(OH^{-})}$=10-2mol/L的溶液中:Na+、NH4+、Cl-、NO3- | |
| C. | c(Fe3+)=0.1mol/L的溶液中:K+、SCN-、SO42-、Cl- | |
| D. | 由水电离的$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-14mol/L的溶液中:Na+、AlO2-、HCO3-、OH- |
18.下列反应中需加入还原剂才能进行的是( )
| A. | Cl2→ClO- | B. | Zn→Zn2+ | C. | H+→H2 | D. | CuO→CuCl2 |
19.下列关于物质的结构和性质的说法正确的是( )
| A. | 因为NaCl溶液导电,所以NaCl晶体中含有离子键 | |
| B. | 因为N的最外层电子数为5,所以N2中有3个非极性共价键 | |
| C. | 因为NH4Cl全部由非金属元素组成,所以NH4Cl是共价化合物 | |
| D. | 因为Na2O2中的原子个数比是1:1,所以离子个数比也是1:1 |