题目内容
【题目】人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农生产及日常生活方面用途非常广泛。试回答下列问题。
(1)Cu+的核外电子排布式为___________________________________;
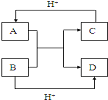
(2)铜镁合金是一种储氢材料,某种铜镁互化物晶胞结构如图,则该互化物的化学式为___________;

(3)叠氮化铜[Cu(N3)2]是一种紫黑色粉末,易爆炸,与N3-互为等电子体的分子有___________(举2例).
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO![]() OHC-CH2CH2OH;
OHC-CH2CH2OH;
OHC-CH2CH2OH中碳原子杂化方式有___________,乙炔属于___________(填“极性”或“非极性”)分子.
(5)若向盛有CuSO4溶液的试管里加入氨水,首先形成蓝色难溶物,继续加入氨水,难溶物溶解,变成蓝色透明溶液,这时得到一种称溶质的化学式为___________,其中含有的化学键类型有______________________;
(6)已知铜镁互化物晶胞参数为apm,则该晶胞的密度为_______________。
【答案】(1)[Ar]3d10或1s22s22p63s23p63d10(2) MgCu2 (3)CO2、N2O (4) sp2、sp3 非极性(5)[Cu(NH3)4]SO4 离子键、共价键(极性键)、配位键 (6)![]() g/cm3
g/cm3
【解析】
试题分析:(1)铜为29号元素,根据原子核外电子排布规律可以写出Cu+的核外电子排布式为1s22s22p63s23p63d10;
(2)根据铜镁互化物晶胞结构,利用均摊法可知,在晶胞中含有铜原子数为8,镁原子数为8×+6×=4,所以铜原子与镁原子数目之比为2:1,据此写出化学式为MgCu2;
(3)N3-中有价电子数为16,三个原子,根据等电子体的概念可知,与N3-互为等电子体的分子有CO2、N2O等;
(4)OHC-CH2CH2OH中两种碳,一种是醛基中的碳,含C=O键,还有一种碳都以单键与其它原子相连,所以碳原子杂化方式有两种,即sp2、sp3,乙炔是直线型对称的分子,所以是非极性分子;
(5)根据名称硫酸四氨合铜,可以写出化学式为:[Cu(NH3)4]SO4,在硫酸四氨合铜中,N、H原子之间以共价键结合,Cu2+提供空轨道,N原子提供孤对电子,则以配位键结合,而硫酸根离子与四氨合铜配离子之间是离子键;
(6)铜镁互化物晶胞中含有4个MgCu2,参数为apm=a×10-9cm,晶胞的体积为a3×10-27cm3,则该晶胞的密度为![]() =
=![]() g/cm3。
g/cm3。

 名校课堂系列答案
名校课堂系列答案