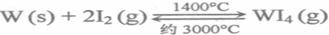题目内容
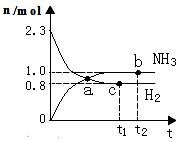
在恒温恒压容器充入一定量N2和H2进行反应:N2(g) + 3H2(g) 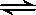 2NH3(g),若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中正确的是
2NH3(g),若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中正确的是
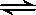 2NH3(g),若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中正确的是
2NH3(g),若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中正确的是
| A.a点表示NH3生成速率与NH3分解速率相等 |
| B.b点H2的转化率大于c点 |
| C.若在t1时刻再充入一定量稀有气体,达到新平衡时n (H2)大于0.8mol |
| D.若在t2时刻再充入一定量NH3(g),达到新平衡时NH3体积分数减少 |
C
试题分析: N2(g) + 3H2(g)
 2NH3(g)
2NH3(g)A.a点表示NH3浓度与NH3浓度相等;
B.b点和c点相比平衡不移动,b点H2的等于c点的转化率;
C.若在t1时刻再充入一定量稀有气体,因为恒压,相当于减压,所以平衡向逆向移动。所以达到新平衡时n (H2)大于0.8mol,正确;
D.若在t2时刻再充入一定量NH3(g),因为恒压,达到新平衡时NH3体积分数不变;
故选C。
点评:恒温恒压下,加入无关气体,体积会增大,相当于减压。平衡会向体积增大的方向移动。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案
相关题目
 PC(g)+qD(g),右图表示A的转化率与压强、温度的关系。由此得出的正确结论是
PC(g)+qD(g),右图表示A的转化率与压强、温度的关系。由此得出的正确结论是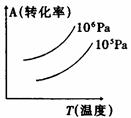
 2SO3(g),下图表示该反应的速率(v)在某一时间(t)段内的变化。则下列时间段中,SO3的百分含量最高的是
2SO3(g),下图表示该反应的速率(v)在某一时间(t)段内的变化。则下列时间段中,SO3的百分含量最高的是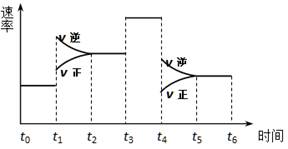
 ?N2O4 ΔH=-57 kJ/mol,
?N2O4 ΔH=-57 kJ/mol,
 2NH3(g)
2NH3(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是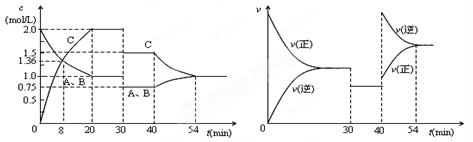
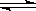 W(s)+3 H2O(g)
W(s)+3 H2O(g)