��Ŀ����
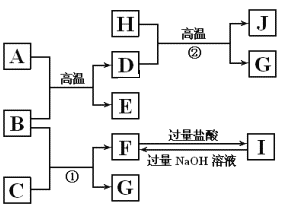
����Ŀ��Ǧ��ұ�����¹������£�
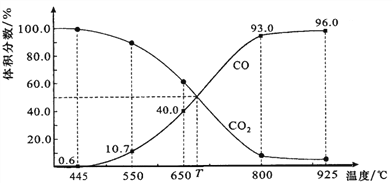
�ٸ���������Ǧ��(PbS)���и�ѡ���ڱ��գ�2PbS+3O2![]() 2PbO+2SO2��
2PbO+2SO2��
���ƴ�Ǧ��PbO +C![]() Pb +CO����PbO+CO
Pb +CO����PbO+CO![]() Pb+CO2��
Pb+CO2��
����˵��������ǣ� ��
A.��ѡ��������Ǧ��Ĺ��̣����������仯
B.��lmolPbSұ����Pb��������������Ҫ12g̼
C.��Ǧ���շ�Ӧ�У�PbS�ǻ�ԭ������ԭ����ֻ��PbO
D.���չ����У�ÿ����lmolPbOת��6mol����
���𰸡�BC
��������
A����ѡ��������Ǧ��Ĺ���û�����������ɣ����������仯��A��ȷ��
B����1molPbSұ����Pb�Ĺ����У����ݷ���ʽ�ó���2PbS~2PbO~C~2Pb��1molPbSұ����Pb������������Ҫ0.5mol��̼������Ҫ6g̼��B����
C����Ǧ���շ�Ӧ2PbS+3O2![]() 2PbO+2SO2�У�PbS��SԪ�ػ��ϼ����ߣ��ǻ�ԭ������Ԫ�ػ��ϼ۽��ͣ���ԭ������PbO��SO2��C����
2PbO+2SO2�У�PbS��SԪ�ػ��ϼ����ߣ��ǻ�ԭ������Ԫ�ػ��ϼ۽��ͣ���ԭ������PbO��SO2��C����
D�����չ��̣�����Pbԭ���غ㣬1molPbSת��Ϊ1molPbO��Pb���ϼ�û�б仯��Sת�Ƶ�����6mol��D��ȷ��
��ѡBC��

����Ŀ����1L�����ܱ������г���X(g)��Y(g)��������ӦX(g)+Y(g)![]() M(g)+N(g)������ʵ���������±���
M(g)+N(g)������ʵ���������±���
ʵ���� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
n(X) | n(Y) | n(M) | ||
�� | 700 | 0.10 | 0.10 | 0.09 |
�� | 800 | 0.20 | 0.20 | 0.10 |
�� | 800 | 0.20 | 0. 30 | a |
�� | 900 | 0.10 | 0.15 | b |
����˵���������
A. ʵ����У���5minʱ���n(M) =0.05mol����0��5minʱ���ڣ���N��ʾ��ƽ����Ӧ����v(N) =0.01 mol/( L��min)
B. ʵ����У��÷�Ӧ��ƽ�ⳣ��K= 1.0
C. ʵ����У��ﵽƽ��ʱ��X��ת����Ϊ60%
D. ʵ����У��ﵽƽ��ʱ��b>0.06
����Ŀ��Bodensteins�о������з�Ӧ��2HI(g)![]() H2(g)+I2(g) H=+11 kJ��mol-1����716Kʱ�����������е⻯������ʵ�������x(HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
H2(g)+I2(g) H=+11 kJ��mol-1����716Kʱ�����������е⻯������ʵ�������x(HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI�� | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
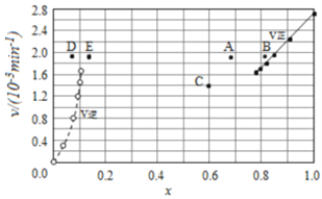
������ʵ�����ݼ���õ�v����x(HI)��v����x(H2)�Ĺ�ϵ������ͼ��ʾ�����ı��������ٴδﵽƽ��ʱ�������й���������ȷ���ǣ�������
A.�������¶ȵ�ijһ�¶ȣ��ٴδﵽƽ��ʱ����Ӧ����ֱܷ���A��E
B.���ı������������ѹǿ���ٴδﵽƽ��ʱ����Ӧ����ı�����ǰ��ͬ
C.���ı��������ʹ�ô������ٴδﵽƽ��ʱ����Ӧ����ı�����ǰ��ͬ
D.���ٴγ���a mol HI����ﵽƽ��ʱ����Ӧ��ĺ�����ֵ���䣬������ֵ����
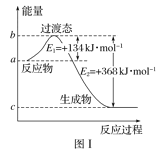
����Ŀ���ο�����ͼ�����й�Ҫ��ش����⣺
��1��ͼ����1molNO2(g)��1molCO(g)��Ӧ����CO2��NO�����������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��___(��������������С����������������ͬ)����H�ı仯��__����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��__��
��2���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)��H2O(g)=CO2(g)��3H2(g) ��H����49.0kJ��mol��1
��CH3OH(g)��![]() O2(g)=CO2(g)��2H2(g) ��H����192.9kJ��mol��1
O2(g)=CO2(g)��2H2(g) ��H����192.9kJ��mol��1
��֪��H2O(g)=H2O(l) ��H����44kJ��mol��1
��״�ȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��___��
��3���±��Dz��ֻ�ѧ���ļ������ݣ�
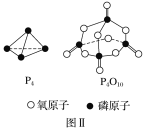
��ѧ�� | P��P | P��O | O=O | P=O |
����/kJ��mol��1 | a | b | c | x |
��֪1mol����(P4)��ȫȼ�շ���ΪdkJ����������ȫȼ�յIJ���ṹ��ͼ����ʾ�������x��___kJ��mol��1(�ú���a��b��c��d�Ĵ���ʽ��ʾ)��