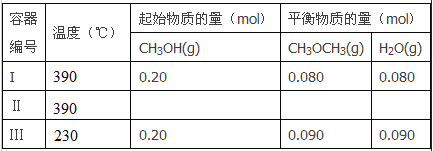
题目内容
【题目】无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为__________________
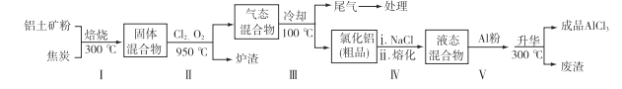
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
已知:
物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1 023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是________(只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是________。
③已知:
Al2O3(s)+3C(s)===2Al(s)+3CO(g)
ΔH1=+1 344.1 kJ·mol-1
2AlCl3(g)===2Al(s)+3Cl2(g)
ΔH2=+1 169.2 kJ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为_______________________。
④步骤Ⅲ的尾气经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为____________。
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是_______________________。
【答案】(1)Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
(2)①防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率
②铁或Fe
③Al2O3(s)+3C(s)+3Cl2(g)===2AlCl3(g)+3CO(g) ΔH=+174.9 kJ·mol-1
④NaCl、NaClO、Na2CO3
⑤除去FeCl3,提高AlCl3纯度
【解析】(1)Al3+水解生成Al(OH)3和H+。
(2)①水分减少可防止Al3+的水解,气孔数目增多,增大了接触面积,可以加快反应速率;②焦炭能还原矿石中的铁;③根据盖斯定律,将第一个反应减去第二个反应可得该热化学反应方程式;④尾气中存在Cl2和CO2,故与NaOH溶液反应生成NaCl、NaClO、Na2CO3;⑤根据工艺流程示意图可知液态混合物中含有FeCl3杂质,因此加入铝粉可除去FeCl3,提高AlCl3的纯度。

 阅读快车系列答案
阅读快车系列答案