题目内容
【题目】一定温度下,在三个体积都为2L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
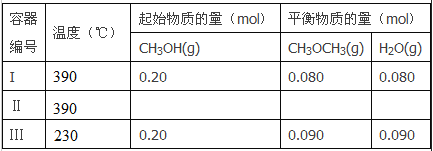
回答下列问题:
(1)反应的△H_________O(填“>”或“<”);判断的理由是_____________。
(2)容器I到达平衡所需的时间为20s,反应速率v(CH3OH)为________mol/(L·s)。390℃时该反应的平衡常数K1=_________(填数值)。
(3)容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,CH3OH起始的物质的量为____________;平衡时CH3OH(g)的体积分数为__________。
(4)390℃,若向3L容器中充入0.9mol CH3OH(g), 0.6mol CH3OCH3(g)和0.3molH2O(g),则起始时该反应速率V正_____________V逆。(填“>”“<”或“=”)
【答案】(1)<;投料量相同时,温度高的容器,平衡时二甲醚的物质的量小,说明反应为放热反应,△H小于0。(2)0.004;4(3)0.40mol;20%(4)>
【解析】
试题分析:(1)根据表格提供的信息,Ⅰ和Ⅲ投料量相同时,温度高的容器,平衡时二甲醚的物质的量小,说明反应为放热反应,△H小于0。
(2)容器I到达平衡所需的时间为20s,平衡时二甲醚的物质的量为0.080mol,根据化学方程式,反应掉的甲醇为0.16mol,则反应速率v(CH3OH)=0.16mol÷(2L×20s)=0.004 mol/(L·s);390℃时该反应达到平衡时,二甲醚的浓度为0.04mol/L,水蒸气的浓度为0.04mol/L,甲醇的浓度为(0.20-0.16)÷2=0.02mol/L,平衡常数K1=(0.04×0.04)÷(0.02×0.02)=4。
(3)该反应是左右气体系数和不变的可逆反应,容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,根据等效平衡理论,Ⅱ中CH3OH起始物质的量为Ⅰ中甲醇起始物质的量的2倍,则CH3OH起始的物质的量为0.40mol,平衡时CH3OH(g)的体积分数与Ⅰ平衡时体积分数相同,为0.04÷0.20×100%=20%。
(4)根据题给数据,Q=(0.1×0.2)÷(0.3×0.3)=0.22<K,平衡正向移动,则起始时该反应速率V正>V逆。

 阅读快车系列答案
阅读快车系列答案