题目内容
根据键能数据估算CH4 (g)+4F2 (g) =CF4+4HF(g)的反应热ΔH为( )
A.–1940 kJ · mol-1 B.1940 kJ · mol-1
C.–485 kJ · mol-1 D.485 kJ · mol-1
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ/mol) | 414 | 489 | 565 | 155 |
C.–485 kJ · mol-1 D.485 kJ · mol-1
A
反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的反应热是4×414 kJ/mol+4×155 kJ/mol-4×489 kJ/mol-4×565 kJ/mol=-1940 kJ/mol.答案选A。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
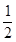 H2(g)+
H2(g)+ 2NH3(g) +
2NH3(g) + 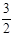 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1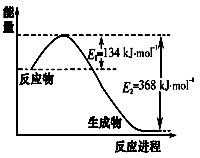
 2NH3(g) △H2=-92.4kJ/mol
2NH3(g) △H2=-92.4kJ/mol