题目内容
【题目】下列氢键从强到弱的顺序正确的是
①O—H…O ②N—H…N ③F—H…F ④O—H…N
A. ①②③④B. ③①④②C. ③②④①D. ③④①②
【答案】B
【解析】
氢键的强度是指X—H…Y分解为X—H和Y所需的能量,X、Y原子半径越小,电负性越大,形成的氢键越强。
氢键可表示为X—H…Y,原子半径:F<O<N,电负性:F>O>N, X、Y原子半径越小,电负性越大,形成的氢键越强,则氢键由强到弱的顺序为:F—H…F> O—H…O> O—H…N> N—H…N,答案选B。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验,并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
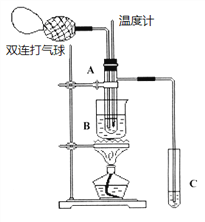
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)____________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A中的位置,在实验开始时,为控制并测量反应溶液的温度,温度计水银球的位置应在_____________;当试管A中的主要反应完成后,为在C中收集乙酸,温度计水银球的位置应在______________,该操作名称为 _____________;烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找);
(3)乙酸是非常重要的工业原料,其氯代物——氯乙酸可在工业上生产食品香精菠萝酯(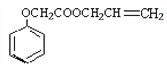 ),实验室模拟工业简易流程如下:
),实验室模拟工业简易流程如下:
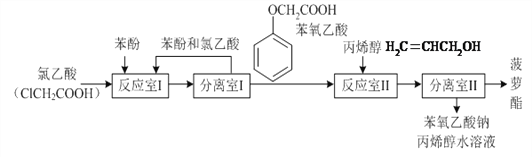
反应室I中发生反应的反应类型是___________。
分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;
洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是__________________________(用化学方程式表示)。
【题目】下物质分类组合正确的是 ( )
A | B | C | D | |
强电解质 | HCl | FeCl3 | H3PO4 | HClO |
弱电解质 | HF | CH3COOH | NH3·H2O | Ba(OH)2 |
非电解质 | C2H5OH | Zn | H2O | SO3 |
A. A B. B C. C D. D