题目内容
【题目】铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______;
(3)SO42-的立体构型是________,其中S原子的杂化轨道类型是_______;
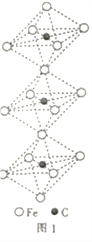
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
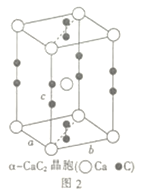
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
【答案】(10分)(1)Cu+2 H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O;
CuSO4+ SO2↑+ 2H2O;
(2)白色无水硫酸铜可与水结合生成蓝色的CuSO4·5 H2O,显示水合铜离子特征蓝色;
(3)正四面体,sp3;(4)6s1; 3:1;金属键;(5)H8AuCu3
【解析】(1)Cu+2 H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O;
CuSO4+ SO2↑+ 2H2O;
(2)白色无水硫酸铜可与水结合生成蓝色的CuSO4·5 H2O,显示水合铜离子特征蓝色;
(3)正四面体,sp3;(4)类比铜原子最外层得:6s1;在晶胞中Cu原子处于面心,6×1/2=3,Au原子处于顶点位置,8×1/8=1,则该合金中Cu原子与Au原子数量之比为3:1;金属键;(5)类比CaF2的晶胞图,Ca2+占据顶点和面心,晶胞内填充4个F-,类比一下,Cu占据面心,Au占据顶点,那H2只能占据晶胞内部的空间了,一个H2分子相当于一个F-,这样看来一个晶胞分摊一个Au原子,3个Cu原子,4个H2分子,所以化学式为AuCu3(H2)4,就是答案上的H8AuCu3。