题目内容
【题目】实验探究是体验知识的产生和形成过程的基本途径。下面是某同学完成的探究实验报告的一部分:实验名称:卤素单质的氧化性强弱比较
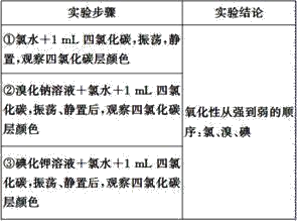
实验药品:溴化钠溶液、碘化钾溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
实验设计如下,请回答:
(1)完成该实验需用到的实验仪器是__、__。
(2)②中反应的化学方程式为__;③中反应的离子方程式为__。
(3)四氯化碳在实验中所起的作用是__。
(4)该同学的实验设计不足之处是__,改进的办法是__。
【答案】试管 胶头滴管 2NaBr+Cl2=2NaCl+Br2 Cl2+2I-=2Cl-+I2 萃取剂 没能比较出溴和碘单质的氧化性强弱 将第③改为碘化钾溶液+溴水+1mL四氯化碳,振荡、静置,观察四氯化碳层的颜色
【解析】
(1)该实验用量筒量取试剂,可在试管中进行反应;
(2)②中反应的化学方程式为 2NaBr+Cl2=2NaCl+Br2;③中反应的离子方程式为2I-+Cl2=2Cl-+I2;
(3)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳;
(4)不能比较溴、碘的氧化性强弱,以此来解答。
由非金属单质间的置换反应来比较单质的氧化性强弱可知,Cl2能置换出Br2、I2,Br2能置换出I2,则说明氧化性Cl2>Br2>I2,
(1)该实验用量筒量取试剂,可在试管中进行反应,还需要胶头滴管滴加液体,
故答案为:试管、胶头滴管;
(2)②中反应的化学方程式为2NaBr+Cl2=2NaCl+Br2;③中反应的离子方程式为2I+Cl2=2Cl+I2,
故答案为:2NaBr+Cl2=2NaCl+Br2;2I+Cl2=2Cl+I2;
(3)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳,所以其作用为萃取剂,使生成的Br2、I2溶于其中,便于观察现象,
故答案为:萃取剂;
(4)设计的实验中不能证明溴的氧化性强于碘,把第③步改为:KI溶液+溴水+1mLCCl4,振荡,静置,观察CCl4层颜色,
故答案为:没有比较Br2和I2的氧化性强弱;把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是否变蓝色(或KI溶液+溴水+1mLCCl4,振荡,静置,观察四氯化碳层颜色)。