题目内容
16.透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶.制备它的一种配方中含有下列四种物质: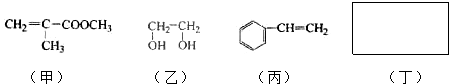
填写下列空白:
(1)甲中不含氧原子的官能团是碳碳双键;下列试剂能与甲反应而褪色的是ac(填标号)
a.Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:CH2=CH-CH2-CH2-COOH
(3)通过下列转化可以得到乙(其中A、B均为有机物):乙醇一定条件→ABr2/CCl4→B氢氧化钠溶液→乙
A的分子式是CH2=CH2,写出B→乙的化学方程式BrCH2CH2Br+2NaOH→H2O△HOCH2CH2OH+2NaBr.
(4)已知:
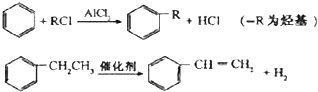
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是
 .
.(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110.丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种.则丁的结构简式为
 .
.
分析 (1)甲含有碳碳双键和酯基等官能团;
(2)一种不含甲基的链状羧酸为CH2=CH-CH2-CH2-COOH;
(3)由乙醇一定条件→ABr2/CCl4→B氢氧化钠溶液→乙可知,乙醇发生消去反应生成A为乙烯、乙烯加成生成B为1,2-二溴乙烷,B水解生成C为乙二醇;
(4)发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、
、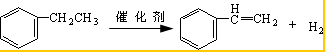 ;
;
(5)丁与FeCl3溶液作用显现特征颜色,且丁的核磁共振氢谱图象仅有2个波峰,强度比为2:1,说明分子中含有酚羟基,分子结构对称.
解答 解:(1)甲含有碳碳双键和酯基等官能团,不含氧的官能团为碳碳双键,含双键、与溴水、高锰酸钾反应褪色,故答案为:碳碳双键;ac;
(2)甲的同分异构体中不含甲基的链状羧酸为CH2=CH-CH2-CH2-COOH,故答案为:CH2=CH-CH2-CH2-COOH;
(3)由乙醇一定条件→ABr2/CCl4→B氢氧化钠溶液→乙可知,乙醇发生消去反应生成A为CH2=CH2,乙烯加成生成B为1,2-二溴乙烷,B水解生成C为乙二醇,则B→乙的化学方程式为BrCH2CH2Br+2NaOH→H2O△HOCH2CH2OH+2NaBr,故答案为:CH2=CH2;BrCH2CH2Br+2NaOH→H2O△HOCH2CH2OH+2NaBr;
(4)发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、发生反应分别为CH2=CH2+HCl→CH3CH2Cl、
、发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、
、 ,
,
其中属于取代反应的为 ,故答案为:
,故答案为: ;
;
(5)丁与FeCl3溶液作用显现特征颜色,且丁的核磁共振氢谱图象仅有2个波峰,强度比为2:1,说明分子中含有酚羟基,分子结构对称,应为 ,相对分子质量为110,
,相对分子质量为110,
故答案为: .
.
点评 本题考查有机物的合成与推断,侧重于有机物官能团的性质的考查,为高考常见题型,难度不大,注意把握有机物官能团的性质.

 全能测控一本好卷系列答案
全能测控一本好卷系列答案| A. | 周期表中第VA族元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| B. | O2−2与S2-具有相同的质子数和电子数 | |
| C. | 氕、氘、氚分别与O原子形成的水H2O、D2O、T2O的化性质不同 | |
| D. | 形成离子键的阴阳离子间只存在静电吸引力 |

| A. | (3)(4)(2)(1) | B. | (3)(1)(4)(2) | C. | (4)(3)(1)(2) | D. | (3)(4)(1)(2) |
| A. | Na2S溶液使酚酞试液变红:S2-+2H2O?2OH-+H2S | |
| B. | 用右图装置电解CuSO4溶液:2Cu2++2H2O电解_2Cu+O2↑+4H+ | |
| C. | NaHCO3溶液使酚酞试液变红:HCO3-+H2O?H3O++CO32- | |
| D. | 用AlCl3溶液使石蕊试液变红:Al3++3H2O?Al(OH)3+3 H+ |

 ;A→F
;A→F .
.
 ;(B)
;(B) .
.
 .
.