题目内容
【题目】下列各表述与示意图一致的是( )
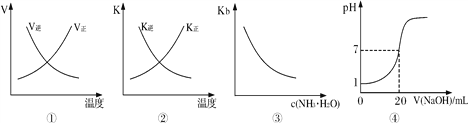
A. 图①表示反应N2(g)+O2(g)![]() 2NO(g) △H>0正、逆反应的速率随温度的变化
2NO(g) △H>0正、逆反应的速率随温度的变化
B. 图②表示反应N2(g)+3H2(g)![]() 2NH3(g) △H<0正、逆反应的平衡常数随温度的变化
2NH3(g) △H<0正、逆反应的平衡常数随温度的变化
C. 图③表示氨水的电离平衡常数随氨水浓度c(NH3·H2O)的变化
D. 图④表示25℃时,用0.1 mol·L-1NaOH溶液滴定20mL 0.l mol·L-1盐酸,溶液的pH随加入碱体积的变化
【答案】D
【解析】A、该反应为吸热反应,温度升高,正逆反应速率都增大,平衡向着正向移动,所以正反应速率大于逆反应速率,而图象中达到平衡后升高温度,逆反应速率减小是错误的,逆反应速率也应该增大,选项A错误;B、该反应为放热反应,升高温度后平衡向着逆向移动,所以逆反应的平衡常数增大,正反应的平衡常数减小,而图象中达到平衡后升高温度,逆反应的平衡常数减小、正反应的平衡常数增大与实际不相符,选项B错误;C、氨水的电离平衡常数与浓度没有关系,只受温度的影响,所以温度不变,电离平衡常数不变,而图象中平衡常数随着氨水的浓度增大而减小是错误的,选项C错误;D、25℃时,用0.1molL-1NaOH溶液滴定20mL 0.lmolL-1盐酸,滴定前盐酸的pH=1,随着氢氧化钠体积不断增大,溶液的pH逐渐增大,当加入20mL氢氧化钠溶液时,二者恰好反应,溶液的pH=7,该图象符合反应实际,选项D正确。答案选D。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】市场销售的某种精制食用盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+KI+H2SO4=K2SO4+I2+H2O,______________
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应后溶液显酸性,写出该反应的离子方程式:_____________________________。
②某同学设计回收四氯化碳的操作步骤如下,请将缺少的操作步骤补充完整。
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3溶液
c.____________________ d.分离出下层液体。
(3)已知:I2+2S2O32=2I-+S4O62-。某质量检验监督局测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,以6.0×10-4mol·L-1的Na2S2O3标准溶液滴定,消耗20.00mL标准液。
①判断c中滴定反应恰好完全的现象是_____________________。
②根据以上实验和包装袋说明,所测精制盐的碘含量是____mg/kg。
(4)用惰性电极电解KI溶液可制备碘酸钾,则阳极反应式为_____________________。
【题目】工业上采用FeSO4和NaOH为主要原料、在碱性条件下通入空气氧化沉淀制备铁磁粉Fe3O4,其原理如下:
①FeSO4 +2NaOH==Fe(OH)2↓ +Na2SO4
②4Fe(OH)2+O2 +2H2O= =4Fe(OH)3↓
③Fe(OH)2+2Fe(OH)3![]() Fe3O4+4H2O
Fe3O4+4H2O
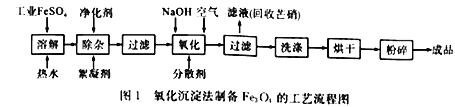
硫酸亚铁在不同温度下的溶解度:
温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
I.(问题讨论)
(1)溶解时,所用热水的温度约为___________,目的是_______________________________________。
(2)副产品芒硝的化学式是_______________________。
(3)为了检验产品是否洗涤干净,需要进行的实险操作是________________________________。
II.(组成确定)
资料显示:①铁的氯氧化物在受热时分解生成铁的氧化物(化合价不变);
②Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4 ,再生成FeO(黑色),最后生成Fe。
为确定用以上方法制得的产品的纯度,称取23.28g该样品利用图2装置进行实验探究。
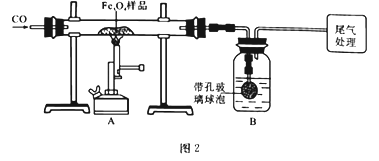
(1)该组同学欲通过称量B装置反应前后的质量变化来计算并确认该样品中的杂质。B中的最佳试剂是________(填字母),B中带孔玻璃球泡的作用是____________________________________。
A.澄清石灰水 B.氢氧化钠浓溶液 C.稀盐酸 D.水
(2)上述实验过程中,CO气体除作为反应物外,能起到的作用还有:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②停止加热后,继续通CO气体,防止生成物被氧化,防止B中的溶液倒吸入A中,还可以_______,以提高实验的精确度。
(3)利用仪器测定并绘制出反应过程中A装置中玻璃管内的固体质量随温度的变化曲线,如图3:

①样品中含有的杂质成分是_____________________(填化学式)。
②样品中杂质的质量分数为_____ %(保留2位小数)。