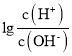题目内容
【题目】常温下联氨![]() 的水溶液中有:
的水溶液中有:
![]()
![]()
![]()
![]() 提示:二元弱碱的电离也是分步电离
提示:二元弱碱的电离也是分步电离![]()
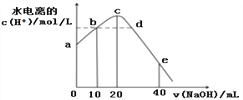
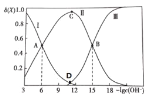
该溶液中的微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是![]()
![]()
A.据A点可求:![]()
B.D点溶液的 ![]()
C.若C点为![]() 溶液,则存在:
溶液,则存在:![]()
D.在![]() 水溶液中,
水溶液中,![]()
【答案】B
【解析】
已知联氨的两步电离分别为:N2H4+H2O![]() N2H5++OH-,N2H5++H2O
N2H5++OH-,N2H5++H2O![]() N2H62++OH-.曲线Ⅰ为N2H4、Ⅱ为N2H5+、Ⅲ为N2H62+;
N2H62++OH-.曲线Ⅰ为N2H4、Ⅱ为N2H5+、Ⅲ为N2H62+;
A.K1= 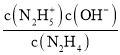 ,A点N2H5+和N2H4的物质的量分数相等,则c(N2H5+)=c(N2H4),K1=c(OH-)=10-6,故A正确;
,A点N2H5+和N2H4的物质的量分数相等,则c(N2H5+)=c(N2H4),K1=c(OH-)=10-6,故A正确;
B.K2=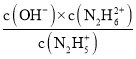 ,B点c(N2H5+)=c(N2H62+),则K2=c(OH-)=10-15;①N2H4+H2O
,B点c(N2H5+)=c(N2H62+),则K2=c(OH-)=10-15;①N2H4+H2O![]() N2H5++OH-,②N2H5++H2O
N2H5++OH-,②N2H5++H2O![]() N2H62++OH-,①+②得N2H4+2H2O
N2H62++OH-,①+②得N2H4+2H2O![]() N2H62++2OH-,则K1×K2=
N2H62++2OH-,则K1×K2=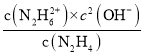 = 10-6×10-15=10-21,在D点c(N2H4)= c(N2H62+),故c(OH-)=
= 10-6×10-15=10-21,在D点c(N2H4)= c(N2H62+),故c(OH-)=![]() =10-10.5,故B错误;
=10-10.5,故B错误;
C.N2H5Cl溶液中存在电荷守恒:c(OH-)+c(Cl-)=c(H+)+c(N2H5+)+2c(N2H62+),C点显酸性,c(H+)>c(OH-),c(Cl-)>(N2H5+)+2c(N2 H62+),故C正确;
D.在N2N5Cl的水溶液中,存在电荷守恒c(OH-)+c(Cl-)=c(H+)+c(N2H5+)+2c(N2H62+)和物料守恒:c(Cl-)=c(N2H4)+c(N2H5+)+c(N2H62+),则c(OH-)+ c(N2H4)+c(N2H5+)+c(N2H62+)=c(H+)+c(N2H5+)+2c(N2H62+)得c(OH-)+ c(N2H4)=c(H+)+ c(N2H62+),故D正确;
故答案为B。

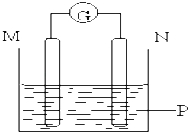
【题目】如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
M | N | P | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸溶液 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A.A B.B C.C D.D