��Ŀ����
����Ŀ��̼���仯����㷺��������Ȼ�硣��ش��������⣺
��1�������ǵ�����̼Ԫ�ص�������ճء�
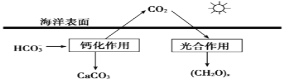
�����ں�ˮ�е�CO2��Ҫ��������̼��ʽ���ڣ�����CO2��H2CO3��___________��___________��
���ں���̼ѭ���У���ͨ������ͼ��ʾ��;����̼��д���ƻ����õ����ӷ���ʽ___________��
��2������CO2�ܽ��ں�ˮ��ʹ���ຣ���������پ���в���о������������ͼ��ʾ�����Ӻ�ˮ����ȡCO2�����Խ��ͻ�����������CO2�ĺ�����
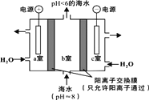
�� a�ҵĵ缫��Ӧʽ��__________��
�� ���ø�װ�ò���������X�ɴ���b���ų��ĺ�ˮ����ÿ��Żشĺϸ�ˮ��X�Ļ�ѧʽ��__________��
��3����֪��NH3��H2O��Kb=1.7��10��5��H2CO3��Ka1=4.3��10��7��Ka2=5.6��10��11����ҵ����β���е�CO2������֮һ�ǰ�ˮ��Һ���ռ��������������ǽ�������ȴ��15.5�桫26.5����ð�ˮ���չ�����CO2��������Һ��pH___________7�����������=������������������ȴ��15.5�桫26.5��Ŀ���ԭ����____________��
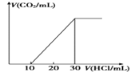
��4��Ϊ�˲���ij��ˮ����̼��������ȡ100mL��ˮ���ữ����N2����CO2������NaOH��Һ���ա�������Һ�еμ�1.0mol/L���ᣬ���ɵ�V(CO2)��V(����)�仯��ϵ��ͼ��ʾ����ԭ����Һ������Ũ���ɴ�С��˳��Ϊ__________��
���𰸡�HCO3�� CO32- ![]() 2H2O - 4e- = O2�� + 4H+��4OH--4e-= O2��+2H2O NaOH �� �������չ����а�ˮ�Ļӷ����ٽ���ˮ��CO2������ c(Na+)> c(HCO3-) > c(CO32-) > c(OH-) > c(H+)
2H2O - 4e- = O2�� + 4H+��4OH--4e-= O2��+2H2O NaOH �� �������չ����а�ˮ�Ļӷ����ٽ���ˮ��CO2������ c(Na+)> c(HCO3-) > c(CO32-) > c(OH-) > c(H+)
��������
(1)�ٶ�����̼����ˮ����̼�ᣬ̼��Ϊ���ᣬ���ֵ�������̼�����������ͼ��֪�˹���̼�����ת������̼��ƣ��ݴ���д����ʽ��
(2)��a�ҽӵ�Դ��������Ϊ������ˮʧȥ�������������������ӣ��ڸ��ݵ��ԭ�������ж������
(3)�÷�Ӧ��һˮ�ϰ��Ͷ�����̼��Ӧ����̼����泥����ݵ���ƽ�ⳣ�������ж�̼�������Һ������ԣ������¶ȶ�һˮ�ϰ��Ͷ�����̼��Ӱ��������
(4)����ͼ���֪������̼���ƺ�̼��������Һ��̼���ƺ�̼���������ʵ���֮��Ϊ1��1���������ˮ���ԭ���������
(1)�ٶ�����̼����ˮ���ɵ�̼��Ϊ���ᣬ���ֵ�������̼��������йط���ʽΪ��CO2+H2OH2CO3��H2CO3H++HCO3-�����ں�ˮ�е�CO2��Ҫ��������̼��ʽ���ڣ�����CO2��H2CO3��HCO3-��CO32-���ʴ�Ϊ��HCO3-��CO32-��
�ڷ�Ӧ���к���̼�������������Ϊ̼��ƣ�����Ԫ���غ��Լ�����غ�ó�����ʽΪ��
2HCO3-+Ca2+=CaCO3��+CO2��+H2O���ʴ�Ϊ��2HCO3-+Ca2+=CaCO3��+CO2��+H2O��
(2)��a�ҽӵ�Դ��������Ϊ������ˮʧȥ�������������������ӣ��缫��ӦʽΪ2H2O-4e-=4H++O2����4OH--4e-= O2��+2H2O���ʴ�Ϊ��2H2O-4e-=4H++O2����4OH--4e-= O2��+2H2O��
��c�ҽӵ�Դ�ĸ�����Ϊ������ˮ�õ������������������������ӣ���ˮ�к��д���Na+��ͨ�������ӽ���Ĥ�����c������NaOH�����������ƴ���b���ų��ĺ�ˮ(pH��6�ĺ�ˮ)����ÿ��Żشĺϸ�ˮ���ʴ�Ϊ��NaOH��
(3)���������ǽ�������ȴ��15.5��26.5�����ð�ˮ���չ�����CO2���÷�Ӧ��һˮ�ϰ��Ͷ�����̼��Ӧ����̼����泥���Ӧ�Ļ�ѧ����ʽΪ��NH3��H2O+CO2=NH4HCO3������NH3��H2O��Kb=1.7��10��5��H2CO3��Ka1=4.3��10��7��Ka2=5.6��10��11��֪̼��������ӵ�ˮ��̶�(Kh=![]() =
=![]() ��10��3)����笠����ӵ�ˮ��̶�(Kh=
��10��3)����笠����ӵ�ˮ��̶�(Kh=![]() =
=![]() ��10��9)����Һ�Լ��ԣ�pH��7��������ȴ��15.5��26.5�������Խ������չ����а����ӷ����ٽ���ˮ�Զ�����̼�ijɷ����գ��ʴ�Ϊ�������������չ����а����ӷ����ٽ���ˮ�Զ�����̼�ijɷ����գ�
��10��9)����Һ�Լ��ԣ�pH��7��������ȴ��15.5��26.5�������Խ������չ����а����ӷ����ٽ���ˮ�Զ�����̼�ijɷ����գ��ʴ�Ϊ�������������չ����а����ӷ����ٽ���ˮ�Զ�����̼�ijɷ����գ�
(4)Ϊ�˲���ij��ˮ����̼��������ȡ100mL��ˮ���ữ���� N2����CO2������NaOH��Һ���գ�������Һ�еμ�1.0mol/L���ᣬ���ܷ����ķ�Ӧ�Ⱥ�ΪNaOH+ HCl=NaCl+H2O��Na2CO3 + HCl = NaHCO3 +NaCl��NaHCO3 + HCl=NaCl+H2O��CO2��������ͼ���֪����Һ�к���̼�����ƺ�̼���ƣ��Ҷ������ʵ���֮��Ϊ1��1������ˮ�⣬��Һ�Լ��ԣ���Һ������Ũ�ȴ�СΪ��c(Na+)��c(HCO3-)��c(CO32-)��c(OH-)��c(H+)���ʴ�Ϊ��c(Na+)��c(HCO3-)��c(CO32-)��c(OH-)��c(H+)��

 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�����Ŀ������ʵ���У�ʵ�������۶���ȷ�����߾��������ϵ����
ʵ�� | ���� | ���� | |
A | ��Ba(NO3)2��Һ��ͨ������������� | �а�ɫ�������� | SO2��Ba(NO3)2��Ӧ�õ�BaSO3 |
B | ��FeI2����Һ�еμ���������ˮ | ��Һ��ɫ���� | Cl2��Fe2+��Ӧ����Fe3+ |
C | ��������Һ�мӼ���ϡ���ᣬˮԡ����5min���ټ�����Cu(OH)2����� | ��ש��ɫ�������� | ����û��ˮ�� |
D | ���з�̪��Na2CO3��Һ�м�������BaCl2���� | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
A. A B. B C. C D. D
����Ŀ��2SO2(g) + O2(g) ![]() 2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
�� | �� | �� | ||
��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2��ƽ��ת���� / % | 80 | ��1 | ��2 | |
A. ���з�Ӧ��ƽ�ⳣ��С����
B. ƽ��ʱ������c(SO3)�Ǽ��е�2��
C. ���¶��£�ƽ�ⳣ��ֵΪ400
D. ƽ��ʱ������O2��ת���ʴ�������O2��ת����
����Ŀ��A��B��C��D��E��F��G��H��Ԫ�����ڱ�ǰ�����ڳ���Ԫ�أ���ԭ���������������������Ϣ���±���
Ԫ�� | �����Ϣ |
A | ԭ�Ӻ�����6�ֲ�ͬ�˶�״̬�ĵ��� |
C | ��̬ԭ����s����������p����������� |
D | ԭ�Ӱ뾶��ͬ����Ԫ������� |
E | ��̬ԭ�����������Ų�ʽΪ3s23p1 |
F | ��̬ԭ�ӵ������p������������ӵ������������������ӵ����������෴ |
G | ��̬ԭ�Ӻ�����7���ܼ���������ߵ��ܼ�����6������ |
H | ���ҹ�ʹ������ĺϽ��е�����ҪԪ�� |
���û�ѧ������գ�
(1) AԪ����Ԫ�����ڱ��е�λ��________��A��B��C����Ԫ�صĵ�һ�������ɴ�С������Ϊ_____����Ԫ�ط�����д����
(2) BԪ���������к�����ḻ��Ԫ���γɵ��������ķ��ӹ���Ϊ____��BԪ�����γɵĵ��ʷ�����������������Ŀ֮��Ϊ____��
(3) GԪ�صĵͼ������ӵ����ӽṹʾ��ͼ��________��FԪ��ԭ�ӵ���Χ�����Ų�ͼ��________��HԪ�صĻ�̬ԭ�Ӻ�������Ų�ʽ��________��
(4) DԪ�صĵ��ʼ��䳣�����������ɫ��Ӧ��Ҫ������ԭ�ӹ����е�______��A.ԭ�����չ���B.ԭ�ӷ�����ף�
(5) ����Ԫ������p������_______����Ԫ�ط�����д����