��Ŀ����
����Ŀ��A��B��C��X��Y��Z��Ԫ�����ڱ��е�ǰ20��Ԫ�أ���ԭ����������������֪���ǵIJ��ֻ�������������£�
A�� �⻯�� | B�� �⻯�� | C�� �⻯�� | X�� ������ | Y���⻯�� ���ӹ��� | Zԭ�� |
��������� ���л��� | ˮ��Һ �ʼ��� | ˮ��Һ ������ | ���� ������ | �������� | �۵����Ų�Ϊ4s2 |
�ش��������⣺
(1)д����ӦԪ�ص�������A__________��B__________��C__________��X__________��Y__________��Z__________
(2)X��Y��Z����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳���ǣ���Ԫ�ط��ź���>����ʾ����__________
(3)д��B���⻯����C���⻯�ﷴӦ��������ĵ���ʽ��__________��
(4)��֪C�ĵ�������ˮ�в���һ�ֳ����������Ե��ʣ���д���÷�Ӧ�Ļ�ѧ����ʽ��
__________��
(5)�ԱȽ�A��Y������������۵�ĸߵͣ��þ������ʻ�ѧʽ��">"��"<"��"="��ʾ����__________��˵������__________��
���𰸡� ̼ �� �� �� �� �� Ca �� Al�� Si 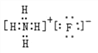 2F2 + 2H2O = 4HF + O2 CO2�� SiO2 CO2Ϊ���Ӿ��壬�ɷ��Ӽ���������ϣ���SiO2Ϊԭ�Ӿ��壬�ɹ��ۼ���ϡ����ۼ�ǿ�ȴ��ڷ��Ӽ�����������SiO2�۵��CO2���۵�ߡ�
2F2 + 2H2O = 4HF + O2 CO2�� SiO2 CO2Ϊ���Ӿ��壬�ɷ��Ӽ���������ϣ���SiO2Ϊԭ�Ӿ��壬�ɹ��ۼ���ϡ����ۼ�ǿ�ȴ��ڷ��Ӽ�����������SiO2�۵��CO2���۵�ߡ�
��������A�Ǻ�������ߵ��л��ӦΪCH4����AΪCԪ�أ�B������⻯��ˮ��Һ�ʼ��ԣ�ӦΪNH3����BΪNԪ�أ�C���⻯��ˮ��Һ�����ԣ�����ΪF��S��Cl�����ʵĶ�Ӧ���⻯�X��������Ϊ���������Ϊ������������XΪAlԪ��������ԭ������������������CΪFԪ����Y������⻯����ӹ������������壬ӦΪSiԪ����Z�ļ۵����Ų�Ϊ4s2��ӦΪCaԪ�ء�
(1)�������������� AΪCԪ�أ� BΪNԪ�أ�CΪFԪ�أ� XΪAlԪ�أ�YΪSiԪ�أ�ZΪCaԪ�أ��ʴ�Ϊ��̼�� ���� ���� ���� �� �� �ƣ�
(2)һ����ԣ����Ӳ���Խ�࣬ԭ�Ӱ뾶Խ���Ӳ�����ͬ��ԭ������Խ��ԭ�Ӱ뾶ԽС��X��Y��Z����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳����Ca �� Al�� Si���ʴ�Ϊ��Ca �� Al�� Si��
(3)B���⻯����C���⻯�ﷴӦ��������Ϊ����泥��������ӻ��������ʽΪ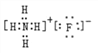 ���ʴ�Ϊ��
���ʴ�Ϊ��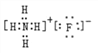 ��
��
(4)������ˮ��Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ2F2 + 2H2O = 4HF + O2���ʴ�Ϊ��2F2 + 2H2O = 4HF + O2��
(5)CO2Ϊ���Ӿ��壬�ɷ��Ӽ���������ϣ���SiO2Ϊԭ�Ӿ��壬�ɹ��ۼ���ϡ����ۼ�ǿ�ȴ��ڷ��Ӽ�����������SiO2�۵��CO2���۵�ߣ��ʴ�Ϊ��CO2�� SiO2��CO2Ϊ���Ӿ��壬�ɷ��Ӽ���������ϣ���SiO2Ϊԭ�Ӿ��壬�ɹ��ۼ���ϡ����ۼ�ǿ�ȴ��ڷ��Ӽ�����������SiO2�۵��CO2���۵����

����Ŀ��100��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������X�����Y���壬�������·�Ӧ��X(g)��2Y(g) ![]() Z(g)��Ӧ�����вⶨ�IJ������ݼ��±���
Z(g)��Ӧ�����вⶨ�IJ������ݼ��±���
��Ӧʱ��/min | n(X)/mol | n(Y)/ mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
����˵����ȷ����
A. ǰ10 min�ڷ�Ӧ��ƽ������Ϊv(Z)��0.10 mol��L��1��min��1
B. �¶�Ϊ200��ʱ��������Ӧƽ�ⳣ��Ϊ20��������ӦΪ���ȷ�Ӧ
C. ���ܱ���������ɱ䣬�����������䣬�ڴﵽƽ�����С�������Ϊԭ��һ�룬��c(X)��1mol/L
D. ���������������䣬���������ٳ���1.00 mol X�����1.20 mol Y���壬����ƽ���Xת��������