题目内容
9.下列说法中不正确的是( )| A. | 化学反应必然伴随能量变化 | |
| B. | 化学反应中的能量变化主要是由化学键的断裂和形成引起的 | |
| C. | 凡是熵增大的反应都是自发反应 | |
| D. | 要判断反应进行的方向,必须综合考虑体系的焓变和熵变 |
分析 A、化学反应伴化学键的断裂和形成,必然有能量的变化;
B、化学反应中的能量变化主要是由化学键的断裂和形成引起的;
C、反应能否自发进行,不取决于焓变或熵变中的一种;
D、化学反应能否自发进行的判据是:△H-T△S<0.
解答 解:A、化学反应伴化学键的断裂和形成,必然有能量的变化,通常表现为热量的变化,故A正确;
B、由化学键的断裂吸收能量,化学键的形成放出能量,由于吸收的能量和放出的能量不等,化学反应产生了能量变化,故B正确;
C、熵增大的反应有利于反应的自发进行,但是熵增加的反应不一定都是自发反应,故C错误;
D、化学反应能否自发进行的判据是:△H-T△S<0,必须综合考虑体系的焓变和熵变,故D正确;
故选:C.
点评 该题考查了化学反应与能量以及影响化学反应方向的因素是:焓变和熵变,注意化学反应能否自发进行的判据是看△H-T△S是否小于零,必须综合考虑体系的焓变和熵变.

练习册系列答案
相关题目
20.下列离子方程式中,书写正确的是( )
| A. | 将固体CuO加入稀H2SO4中 CuO+2H+=Cu2++H2O | |
| B. | 盐酸滴加在石灰石上 CaCO3+2H+=Ca2++H2CO3 | |
| C. | Ba(OH)2溶液与稀硫酸混合 Ba2++SO42-=BaSO4↓ | |
| D. | 铜片加入稀盐酸中 Cu+2H+=Cu2++H2↑ |
4.在一定温度下的定容密闭容器中发生反应H2(g)+I2(g)?2HI(g),下列能说明反应已经达到平衡状态的是( )
| A. | 容器内每减少1mol I2,同时生成2mol HI | |
| B. | 容器内气体压强不再变化 | |
| C. | 混合气体的颜色不再变化 | |
| D. | 混合气体的密度恒定不变 |
1.下列物质属于高分子化合物的是( )
| A. | 油脂 | B. | 纤维素 | C. | 麦芽糖 | D. | 三硝基甲苯 |
19.下列物质属于同系物的是( )
| A. | O2与O3 | B. | 12C与14C | C. | 甲烷与氯乙烷 | D. | 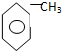 与 与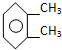 |
