题目内容
1.下列物质属于高分子化合物的是( )| A. | 油脂 | B. | 纤维素 | C. | 麦芽糖 | D. | 三硝基甲苯 |
分析 高分子化合物是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化合物,多为高聚物.
解答 解:纤维素属于高聚物,相对分子质量在一万以上,而油脂、麦芽糖、三硝基甲苯的相对分子质量较小,不属于高分子化合物,
故选B.
点评 本题考查高分子化合物知识,题目难度不大,注意把握高分子化合物的概念和性质.

练习册系列答案
相关题目
11.既可用来鉴别乙烷和乙烯,又可用来除去乙烷中的乙烯以取得纯净乙烷的方法是( )
| A. | 通过足量的溴水 | B. | 通入酸性高锰酸钾溶液 | ||
| C. | 在一定条件下通入氢气 | D. | 与足量的液溴反应 |
12.下列关于有机物的说法正确的是( )
| A. | 聚乙烯可发生加成反应 | |
| B. | 光导纤维、棉花、油脂都是由高分子化合物组成的物质 | |
| C. | 煤油可由石油分馏获得,可用作燃料和保存少量金属钠 | |
| D. | 乙烯和苯都能使溴水褪色,褪色的原因相同 |
9.下列说法中不正确的是( )
| A. | 化学反应必然伴随能量变化 | |
| B. | 化学反应中的能量变化主要是由化学键的断裂和形成引起的 | |
| C. | 凡是熵增大的反应都是自发反应 | |
| D. | 要判断反应进行的方向,必须综合考虑体系的焓变和熵变 |
16.已知2Fe2++Br2═2Fe3++2Br-往100mL溴化亚铁溶液中缓慢通入2.24L(标准状况)氯气,反应完成后溶液中有1/3的溴离子被氧化成溴单质.则原溴化亚铁溶液的物质的量浓度为( )
| A. | 1.2mol/L | B. | 0.3mol/L | C. | 1.4mol/L | D. | 无法计算 |
6.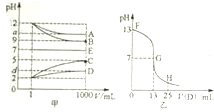 物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1mL稀释到1000mL,pH的变化关系如甲图所示,其中A与D反应得到E.请回答下列问题.
物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1mL稀释到1000mL,pH的变化关系如甲图所示,其中A与D反应得到E.请回答下列问题.
(1)根据pH的变化关系,写出物质的化学式:BNaOH,CHCl.
(2)写出A与C反应的离子方程式:NH3+H+=NH4+.
(3)图乙为室温时向25mL某浓度的B溶液中逐滴滴加0.2mol.L-1的D溶液的过程中pH的变化曲线.
①图乙中B的物质的量浓度为0.1mol.L-1
②G点溶液呈中性,则二者恰好完全反应的点是在FG(填FG、GH)区间.
③G点溶液中各离子浓度大小关系是c(Na+)=c(CH3COO-)>c(H+)=c(OH-).
(4)t℃时,A的稀溶液中c(H+)=10-amol.L-1,c(OH-)=10-bmol.L-1,已知a+b=13,该温度下(t℃),将100mL0.2mol.L-1的C溶液与100mL0.4mol.L-1的B溶液混合后(溶液体积变化忽略不计),溶液的pH=12.
 物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1mL稀释到1000mL,pH的变化关系如甲图所示,其中A与D反应得到E.请回答下列问题.
物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1mL稀释到1000mL,pH的变化关系如甲图所示,其中A与D反应得到E.请回答下列问题.| 阳离子 | NH4+、H+、Na+ |
| 阴离子 | OH-、CH3COO-、Cl- |
(2)写出A与C反应的离子方程式:NH3+H+=NH4+.
(3)图乙为室温时向25mL某浓度的B溶液中逐滴滴加0.2mol.L-1的D溶液的过程中pH的变化曲线.
①图乙中B的物质的量浓度为0.1mol.L-1
②G点溶液呈中性,则二者恰好完全反应的点是在FG(填FG、GH)区间.
③G点溶液中各离子浓度大小关系是c(Na+)=c(CH3COO-)>c(H+)=c(OH-).
(4)t℃时,A的稀溶液中c(H+)=10-amol.L-1,c(OH-)=10-bmol.L-1,已知a+b=13,该温度下(t℃),将100mL0.2mol.L-1的C溶液与100mL0.4mol.L-1的B溶液混合后(溶液体积变化忽略不计),溶液的pH=12.
13.已知某温度时,反应X2(g)+Y2(g)?2XY(g)的平衡常数K=20,由此推测在该温度时,反应2XY(g)?X2(g)+Y2(g)的化学平衡常数为( )
| A. | 20 | B. | 50 | C. | 0.05 | D. | 无法确定 |
10.合成氨工业对国民经济和社会发展具有重要的意义.其原理为:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是②③(填序号).
①反应压强为20Mpa~50Mpa
②500℃的高温
③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中.
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度).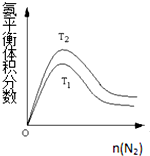
则T2T2<T1T1(填>、=、<),判断的依据是:合成氨反应是放热反应,温度升高,平衡向逆反应方向移动,NH3的体积分数下降,所以T2<T1.
(3)合成氨气所需的氢气可以由水煤气分离得到.涉及反应信息如下:
反应一:C(s)+H2O(g)?H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g)?H2(g)+CO2(g) 平衡常数K2
①K1的表达式:K1=$\frac{c(H2)c(CO)}{c(H2O)}$.
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为0.16mol•L-1•min-1.
(Ⅱ)在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为D(填序号)
A.其它条件不变温度T<900℃
B.其它条件不变温度T>900℃
C.充入一定量氖气
D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2减小(填“增大”、“减小”或“不变”).
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是②③(填序号).
①反应压强为20Mpa~50Mpa
②500℃的高温
③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中.
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度).

则T2T2<T1T1(填>、=、<),判断的依据是:合成氨反应是放热反应,温度升高,平衡向逆反应方向移动,NH3的体积分数下降,所以T2<T1.
(3)合成氨气所需的氢气可以由水煤气分离得到.涉及反应信息如下:
反应一:C(s)+H2O(g)?H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g)?H2(g)+CO2(g) 平衡常数K2
①K1的表达式:K1=$\frac{c(H2)c(CO)}{c(H2O)}$.
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
| 实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
| 3 | T | a | b | c | d | t |
(Ⅱ)在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为D(填序号)
A.其它条件不变温度T<900℃
B.其它条件不变温度T>900℃
C.充入一定量氖气
D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2减小(填“增大”、“减小”或“不变”).
11.下列实验能成功的( )
| A. | 乙醇和浓硫酸加热到140℃制取乙烯 | |
| B. | 乙烷和氯气光照下制取纯净的氯乙烷 | |
| C. | 在苯和溴水的混合物中加入铁粉制取溴苯 | |
| D. | 用酸性高锰酸钾溶液区分 和 和 |