题目内容
7.实验室用NaCl固体配200mL 1.0mol/L NaCl溶液,下列判断不对的是( )| A. | 用托盘天平称取NaCl固体11.7g | |
| B. | 应选用250 mL的容量瓶配制此溶液 | |
| C. | 在转移操作中不慎将溶液洒到容量瓶外面,应该重新配制溶液 | |
| D. | 加蒸馏水至离刻度线1-2 cm时改用胶头滴管定容 |
分析 A.依据m=CVM计算溶质的质量;
B.依据配制溶液的体积及容量瓶的规格选择合适的容量瓶;
C.依据C=$\frac{n}{V}$进行误差分析;
D.依据定容的正确操作解答.
解答 解:A.实验室用NaCl固体配200mL 1.0mol/L NaCl溶液,应选择250ml容量瓶,需要溶质的质量=1.0mol/L×0.25L×58.5g/mol=14.7g/mol,故A错误;
B.实验室用NaCl固体配200mL 1.0mol/L NaCl溶液,应选择250ml容量瓶,故B正确;
C.在转移操作中不慎将溶液洒到容量瓶外面,溶质的物质的量不准确,需要重新配制,故C正确;
D.定容时,加蒸馏水至离刻度线1-2 cm时改用胶头滴管逐滴滴加,到溶液凹液面最低处与刻度线相切,故D正确;
故选:A.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和配制过程是解题关键,注意容量瓶的使用方法,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
5.将干燥的氯气分别通入盛有干花和鲜花的集气瓶后,干花不褪色而鲜花褪色表明( )
| A. | 氯气具有漂白作用 | B. | 鲜花比干花容易衰败 | ||
| C. | 次氯酸见光易分解 | D. | 次氯酸具有漂白作用 |
15.下列物质能用化合反应直接制得的是( )
①FeCl2 ②Fe(OH)3 ③FeCl3 ④Fe(OH)2.
①FeCl2 ②Fe(OH)3 ③FeCl3 ④Fe(OH)2.
| A. | ①③ | B. | ①②③ | C. | ②③ | D. | ②④ |
2.下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
| A. | 除②以外 | B. | 除⑤以外 | C. | 除⑥以外 | D. | 全部 |
19.W、X、Y、Z是短周期元素,它们的核电荷数依次增大.下表列出它们的性质和结构:
(1)元素符号:XO,ZNa.
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式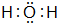 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外S能级上的电子总数与P能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外P能级上的电子总数比S能级上的电子总数多2 |
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式
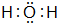 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
16.在同温同压下,下列各组热化学方程式中,△H2>△H 1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g),△H 1;2H2(g)+O2(g)=2H2O(l),△H2 | |
| B. | S(g)+O2(g)=SO2(g),△H 1;S(s)+O2(g)=SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g),△H 1;C(s)+O2(g)=CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g),△H 1;2H2(g)+2Cl2(g)=4HCl(g)△H2 |
17.下列有关反应:4NH3 (g)+5O2 (g)═4NO(g)+6H2O(g)△H (298K)=-905kJ•mol-1 的描述不正确的是( )
| A. | 生成物的总能量小于反应物的总能量 | |
| B. | 该反应为吸热反应 | |
| C. | 该反应为放热反应 | |
| D. | 该反应中每4 mol NH3(g)被氧化,放出905 kJ热量 |