题目内容
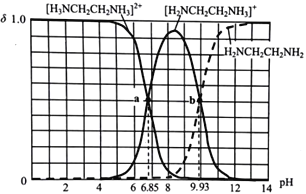
【题目】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )(已知:pH=-lgc(H+))

A.将稀醋酸加水稀释时,c(H+)减小,c(OH-)也减小
B.a、b、c三点溶液的pH:b<a<c
C.a、b、c三点CH3COOH的电离程度:c<a<b
D.a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
【答案】B
【解析】
A.醋酸在溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,将稀醋酸加水稀释时,若平衡不移动,溶液中c(CH3COOH)、c(CH3COO-)、c(H+)减小,加水稀释,平衡正向移动,使c(CH3COO-)、c(H+)在减小的基础上又略有增大,但总的来说c(CH3COO-)、c(H+)减小,由于溶液中存在水的电离平衡,Kw= c(H+)·c(OH-)是定值,所以c(H+)减小,则c(OH-)增大,A错误;
CH3COO-+H+,将稀醋酸加水稀释时,若平衡不移动,溶液中c(CH3COOH)、c(CH3COO-)、c(H+)减小,加水稀释,平衡正向移动,使c(CH3COO-)、c(H+)在减小的基础上又略有增大,但总的来说c(CH3COO-)、c(H+)减小,由于溶液中存在水的电离平衡,Kw= c(H+)·c(OH-)是定值,所以c(H+)减小,则c(OH-)增大,A错误;
B.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,B正确;
C.随水的增多,醋酸的电离的分子数增加,由于醋酸分子总分子数不变,所以醋酸的电离程度在增大,所以a、b、c三点醋酸的电离程度:a<b<c,C错误;
D.a、b、c三点溶液浓度不同,但其中含有溶质的物质的量相同,所以a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积相等,即:a=b=c,D错误;
故合理选项是B。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。已知:CO(g)+H2O(g)H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
(1)上述正向反应是________反应 (填“放热”或“吸热”);
(2)下列条件的改变能加快其反应速率的是_______(选填序号);
①升高温度;②保持体积不变,只增加CO的质量;③保持体积不变,充入Ne使体系压强增大;④保持压强不变,充入Ne使容器的体积增大
(3)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2,发生反应CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如下图所示:
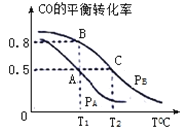
①A、B两点对应的压强大小关系是PA________PB;(填“>”,“<”,“=”)
②A、B、C三点的平衡常数KA、KB、KC的大小关系是 ____________;
③在P1压强、T1℃时,该反应的平衡常数K=___________;
(4)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2:0.2mol CH3OH:0.2mol。此时v正 ____ v逆(填 >、< 或 =)。