题目内容
【题目】下列装置![]() 加持装置略去
加持装置略去![]() 能达到试验目的是( )
能达到试验目的是( )
选项 | A | B | C | D |
装置 |
|
|
|
|
实验目的 | 比较非金属性: N>C>Si | 制备并收集乙酸乙酯 | 除去Ca(OH)2与中的NH4Cl | 验证HCl的溶解性 |
A.AB.BC.CD.D
【答案】D
【解析】
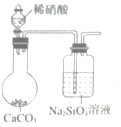
![]() 硝酸易挥发,应除掉二氧化碳中的硝酸,再与硅酸钠反应,否则干扰了检验结果,与题意不符,A错误;
硝酸易挥发,应除掉二氧化碳中的硝酸,再与硅酸钠反应,否则干扰了检验结果,与题意不符,A错误;
B.制备乙酸乙酯时,收集乙酸乙酯的导管不能插入饱和碳酸氢钠溶液中,否则挥发出的乙酸、乙醇易溶于水,会发生倒吸现象,与题意不符,B错误;
C.由于Ca(OH)2与NH4Cl在加热条件下反应生成氨气和氯化钙,无法通过加热除去Ca(OH)2中的NH4Cl,与题意不符,C错误;
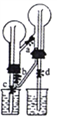
D.HCl溶于水后,烧杯中气体压强小于大气球,气球膨胀,从而可证明HCl的溶解性,符合题意,D正确;
答案为D。

 名校课堂系列答案
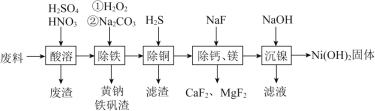
名校课堂系列答案【题目】铈(Ce)是![]() 种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:
种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:

已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。
⑴滤渣的成分是________,反应②的离子方程式是________。
⑵干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为________。两种制备Ce(OH)4的数据如下表:
干法空气氧化法 | 氧化温度 | 氧化率 | 氧化时间 |
暴露空气中 | 110~120 | 90 | 18 |
在对流空气氧化炉中 | 110~120 | 99 | 8 |
在对流空气氧化炉中大大缩短氧化时间的原因是________。
⑶利用电解方法也可以实现铈的回收。
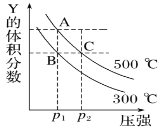
①在酸性条件下电解Ce2O3(如图):阳极电极反应式为________,离子交换膜为________(填“阴”或“阳”)离子交换膜。
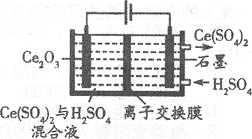
②电解产物Ce(SO4)2是重要的氧化剂,将其配成标准溶液,在酸性条件下能测定工业盐中NaNO2的含量,写出发生反应的离子方程式________。