题目内容
【题目】如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:
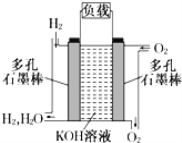
(1)图中通过负载的电子流动方向__(填“向左”或“向右”)。
(2)写出氢氧燃料电池工作时正极电极反应方程式。__。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极电极反应方程式为__。
【答案】向右 2H2O+O2+4e-=4OH- CH4+10OH--8e-=CO32-+7H2O
【解析】
(1)根据原电池工作原理,负极上失电子,电子从负极沿外电路流向正极,所以通过负载的电子流动方向是向右.
故答案为:向右;
(2)正极上氧气得电子和水生成氢氧根离子,发生还原反应,所以电极反应式为2H2O+O2+4e-═4OH-;
故答案为:2H2O+O2+4e-═4OH-;
(3)负极上是燃料失电子,正极上是氧气得电子,所以负极上甲烷反应生成二氧化碳,二氧化碳是酸性氧化物,能和电解质溶液KOH反应生成盐和水,所以负极上的电极反应式为CH4+10OH--8e-═CO32-+7H2O;正极上氧气得电子和水生成氢氧根离子;正负极上的电极反应式相加得总反应方程式,所以总反应方程式为CH4+2O2+2OH-═CO32-+3H2O.
故答案为:CH4+10OH--8e-═CO32-+7H2O。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目