题目内容
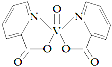
【题目】伞形酮可用作酸碱指示剂,可由雷琐苯乙酮和苹果酸在一定条件下反应制得。下列说法中错误的是
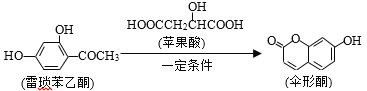
A.1mol伞形酮与足量NaOH溶液反应,最多可消耗3molNaOH
B.1 mol雷琐苯乙酮最多可与4 mol H2发生加成反应
C.苹果酸发生缩聚反应最多可生成2种高分子化合物
D.雷琐苯乙酮在一定条件下可发生氧化、取代、缩聚等反应
【答案】C
【解析】
A.1个酯基水解消耗1molNaOH,水解后生成酚羟基再消耗1molNaOH,分子中的1个酚羟基消耗1molNaOH,所以1mol伞形酮和足量NaOH反应共消耗3molNaOH,A正确;
B.苯环消耗3mol氢气,羰基消耗1mol氢气,共消耗4mol氢气,B正确;
C.可以生成三种高分子化合物,分别为:![]() 、
、![]() 、
、 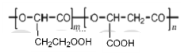 ,C错误;
,C错误;
D.雷琐苯乙酮中羟基能发生氧化反应,羟基、苯环上的H能被取代,有2个羟基,能和多元羧酸发生缩聚反应,D正确。
答案选C。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】研究NO的性质对建设美丽家乡,打造宜居环境具有重要意义。
(1)自然界在闪电时,生成NO的反应方程式为__________________。
(2)T℃时在容积为2L的恒容密闭容器中,充入NO和O2发生反应:2NO(g)+O2(g)2NO2(g),不同时刻测得容器中n(NO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
①在T℃下,0~2s时,该反应的平均反应速率![]() =________;
=________;
②该温度下反应的平衡常数K=________,在T℃下,能提高NO的平衡转化率的措施有_______、________。
(3)已知NO和O2反应的历程如图,回答下列问题:
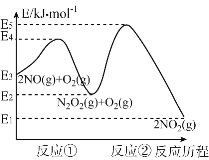
①写出其中反应①的热化学方程式也(△H用含物理量E的等式表示):________。
②试分析上述基元反应中,反应①和反应②的速率较小的是_____(选填“反应①”或“反应②”);已知反应①会快速建立平衡状态,反应②可近似认为不影响反应①的平衡。对该反应体系升高温度,发现总反应速率变慢,其原因可能是____________。