题目内容
【题目】氰气的化学式为![]() ,结构式为
,结构式为![]() ,性质与卤素相似,下列有关叙述正确的是( )
,性质与卤素相似,下列有关叙述正确的是( )
A.氰气分子中既有极性键,又有非极性键
B.氰气分子中![]() 键的键长大于
键的键长大于![]() 键的键长
键的键长
C.氰气分子中含有2个![]() 键和4个
键和4个![]() 键
键
D.氰气不能和氢氧化钠溶液发生反应
【答案】A
【解析】
根据氰气的化学性质与卤素相似分析与化学性质相关问题,再根据元素周期律及成键原则作答。
A.![]() 的结构式为
的结构式为![]() ,N原子与C原子间为极性键,C原子与C原子间为非极性键,故A项正确;
,N原子与C原子间为极性键,C原子与C原子间为非极性键,故A项正确;
B.原子半径越大,键长越长,碳原子半径大于氮原子半径,所以键长:![]() ,因键长:
,因键长:![]() ,键长:
,键长:![]() ,故B项错误;
,故B项错误;
C.氰气分子的结构式为![]() ,该分子中含有3个
,该分子中含有3个![]() 键和4个
键和4个![]() 键,故C项错误;
键,故C项错误;
D.卤素单质能和氢氧化钠溶液反应,氰气的性质和卤素单质的性质相似所以氰气能和氢氧化钠溶液反应,故D项错误;
答案选A。

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
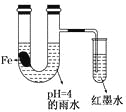
第三学期赢在暑假系列答案【题目】研究NO的性质对建设美丽家乡,打造宜居环境具有重要意义。
(1)自然界在闪电时,生成NO的反应方程式为__________________。
(2)T℃时在容积为2L的恒容密闭容器中,充入NO和O2发生反应:2NO(g)+O2(g)2NO2(g),不同时刻测得容器中n(NO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
①在T℃下,0~2s时,该反应的平均反应速率![]() =________;
=________;
②该温度下反应的平衡常数K=________,在T℃下,能提高NO的平衡转化率的措施有_______、________。
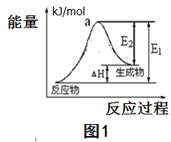
(3)已知NO和O2反应的历程如图,回答下列问题:
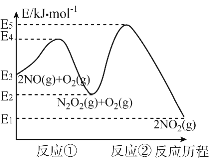
①写出其中反应①的热化学方程式也(△H用含物理量E的等式表示):________。
②试分析上述基元反应中,反应①和反应②的速率较小的是_____(选填“反应①”或“反应②”);已知反应①会快速建立平衡状态,反应②可近似认为不影响反应①的平衡。对该反应体系升高温度,发现总反应速率变慢,其原因可能是____________。