题目内容
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水。实验室以NH4C1、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
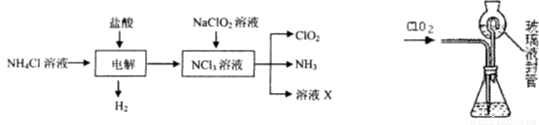
⑴ 写出电解时发生反应的化学方式: 。
⑵ 测定ClO2(如右图)的过程如下:在锥形瓶中加入足最的碘化钾,用100 mL水溶解后,再加3 mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去V mL硫代硫酸钠溶液。
① ClO2通入锥形瓶与酸性碘化钾溶液反应,反应的离子方程式为: 。
② 装置中玻璃液封管的作用是 、 。
③ 滴定至终点的现象是 。
④ 测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)
⑴ NH4Cl+2HCl=3H2↑+NCl3(1分)
⑵ ① 2ClO2+10I-+8H+=2Cl-+5I2+4H2O(1分)
② 用水再次吸收残余的二氧化氯气体,并使锥形瓶内外压强相等(2分)
③ 溶液由蓝色恰好变为无色,且半分钟内不褪色(1分)
④ 1.35cV×10-2 g(1分)
【解析】
试题分析:(1)电解氯化铵和盐酸混合溶液时,根据流程图知生成氢气、和NCl3,其电解反应方程式为:NH4Cl+2HCl 3H2↑+NCl3.
3H2↑+NCl3.
(2)①由题目信息可知,ClO2通入锥形瓶与酸性碘化钾溶液反应,氧化I-为I2,自身被还原为Cl-,同时生成水,反应离子方程式为2ClO2+10I-+8H+=2Cl-+5I2+4H2O,
②装置中玻璃液封管的作用是,用水再次吸收残余的二氧化氯气体,并使锥形瓶内外压强相等.
③淀粉溶液作指示剂,结合反应I2+2S2O32-=2I-+S4O62-可以判断溶液由蓝色恰好变为无色,且半分钟内不褪色,说明滴定至终点。
④VmLNa2S2O3溶液含有Na2S2O3物质的量为V?10-3 L×cmol/L=c?V?10-3 mol.则:
根据关系式:2ClO2~5I2~10Na2S2O3,
2 10
n(ClO2) c?V?10-3 mol
所以n(ClO2)=1/5c?V?10-3 mol.
所以m(ClO2)=1/5c?V?10-3 mol×67.5g/mol=1.35cv×10-2g.
考点:阅读题目获取信息能力、氧化还原反应滴定及应用、对工艺流程及装置理解分析等