题目内容
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
①2Mg+O2 2MgO;②3Mg+N2
2MgO;②3Mg+N2 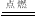 Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2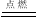 2MgO+C;
2MgO+C;
④Mg+H2O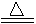 MgO+H2↑; ⑤Mg3N2 +6H2O
MgO+H2↑; ⑤Mg3N2 +6H2O 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
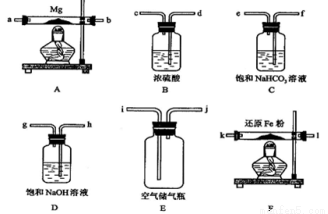
回答下列问题:
(1)在设计实验方案时,除装置A、D、E外,还应选择的装置有 (填字母代号),选择装置D目的为_____________________________ ;
(2)通气后,应先点燃 处的酒精灯;如果同时点燃A、F装置的酒精灯,将会使实验结果 (填“偏高”或“偏低”)原因
(3)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:
_____________________________________________________________________
(1)BF (2分) D 目的是除去空气中的CO2,避免反应③发生;(2分)
(2)F;(1分)偏低;(2分)如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁。(2分)
(3)取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成。(2分)
【解析】
试题分析:(1)该反应中为了得到纯净的氮化镁,必须把影响的产物的气体水,还有氧气去除,装置B是用来除去水蒸汽的,放在A之前,F可以用来除去氧气。D 目的是除去空气中的CO2,避免反应③发生;
(2)这一装置中,很多人可能会考虑到F装置是用来除去水蒸汽的,那样的话,反应产生的氢气怎么办,因此这个装置是用来除去氧气的。如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁。(2分)
(3)验证产物是Mg3N2,必须利用氮化镁的特征反应。取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成。
考点:氮化镁制取的有关知识

 阅读快车系列答案
阅读快车系列答案