题目内容
【题目】(题文)下列关于烷烃的表述正确的是
A. 乙烷的结构式为CH3CH3
B. C5H12分子的某种结构为![]()
C. ![]() 与
与 互为同分异构体
互为同分异构体
D. C4 H10的一氯代物有4种
【答案】D
【解析】
A. CH3CH3是乙烷的结构简式,不是结构式,故A错误; B. 因为C原子最外层只有4个电子,所以在有机结构中C原子周围一定有4个共价键, C5H12分子的某种结构为![]() ,故B错误;C.
,故B错误;C. ![]() 与
与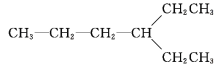 结构相同,属于同种物质。同分异构体是结构不同,分子式相同。故C错误;D.C4H10有2种同分异构体:①CH3—CH2—CH2—CH3、②
结构相同,属于同种物质。同分异构体是结构不同,分子式相同。故C错误;D.C4H10有2种同分异构体:①CH3—CH2—CH2—CH3、②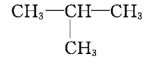 ,①中具有2种位置不同的H原子,所以一氯代物有2种,②中3个—CH3上的H原子完全等同,另一个C原子上的H原子与—CH3上的H原子位置不同,所以一氯代物也有2种,则C4H10的一氯代物共有4种,故D正确;答案:D。
,①中具有2种位置不同的H原子,所以一氯代物有2种,②中3个—CH3上的H原子完全等同,另一个C原子上的H原子与—CH3上的H原子位置不同,所以一氯代物也有2种,则C4H10的一氯代物共有4种,故D正确;答案:D。

 阅读快车系列答案
阅读快车系列答案【题目】工业上利用N2和H2可以实现合成氨气,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列有关问题:
(1)已知N2(g)+O2(g)=2NO(g) ΔH =+180.5kJ·mol-1,N2(g)+3H2(g)![]() 2NH3(g) ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为___________。
2NH3(g) ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为___________。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g),其化学平衡常数K与温度t的关系如下表:
2NH3(g),其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | ...... |
K/(mol/L)2 | 4.1×106 | K1 | K2 | ...... |
完成下列问题:
①比较K1、K2的大小:K1______K2(填“>”、“=”或“<”);
②在恒温恒压下判断该反应达到化学平衡状态的依据是______(填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2) (正)=v(H2) (逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)硝酸工业的尾气NO可用于制备NH4NO3,其工作原理如图。
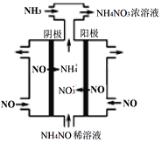
①其阴极的电极反应式为___________。
②常温下,1L pH=6的NH4NO3溶液中c(NH3·H2O)+c(OH-)=________mol·L-1。
(4)工业上生产尿素的化学方程式为:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2,反应达到平衡时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3mol NH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。再次平衡后,平衡常数为______。
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2,反应达到平衡时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3mol NH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。再次平衡后,平衡常数为______。