题目内容
16.现有乳酸(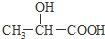 )和乙醇的混合物共1mol,完全燃烧生成54g水和56L(标准状况下测定)CO2,则完全燃烧时消耗氧气物质的量是( )
)和乙醇的混合物共1mol,完全燃烧生成54g水和56L(标准状况下测定)CO2,则完全燃烧时消耗氧气物质的量是( )| A. | 2 mol | B. | 2.25 mol | C. | 3 mol | D. | 3.75 mol |
分析 乳酸分子式为C3H6O3,1mol乳酸完全燃烧耗氧量为(3+$\frac{6}{4}$-$\frac{3}{2}$)mol=3mol,乙醇的分子式为C2H6O,1mol乙醇完全燃烧耗氧量为(2+$\frac{6}{4}$-$\frac{1}{2}$)mol=3mol,二者耗氧量相等,故物质的量一定,二者以任意比混合完全燃烧耗氧量为混合物的3倍.
解答 解:乳酸分子式为C3H6O3,1mol乳酸完全燃烧耗氧量为(3+$\frac{6}{4}$-$\frac{3}{2}$)mol=3mol,
乙醇的分子式为C2H6O,1mol乙醇完全燃烧耗氧量为(2+$\frac{6}{4}$-$\frac{1}{2}$)mol=3mol,
二者耗氧量相等,故物质的量一定,二者以任意比混合完全燃烧耗氧量为混合物的3倍,
故1mol乳酸与乙醇的化合物完全燃烧消耗氧气为1mol×3=3mol,
故选C.
点评 本题考查混合物的有关计算,难度中等,注意利用燃烧通式中耗氧量解答判断.

练习册系列答案
相关题目
6.下列反应属于吸热反应的是( )
| A. | 金属镁与盐酸反应 | B. | 石灰石高温分解 | ||
| C. | 盐酸与氢氧化钠溶液反应 | D. | 二氧化硫和氧气生成三氧化硫 |
7.某学生为了探究锌与盐酸反应过程中的速率变化.在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如表:
(1)解释2min~3min反应速率最大的原因该反应是放热反应,2min~3min时溶液温度最高,反应速率最快;反应速率最小的时间段是4min~5min,原因为此时反应物的浓度最小,反应速率最慢.
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50.0 | 120.0 | 232.0 | 290.0 | 312.4 |
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
4.高温下,炽热的铁与水蒸气在一个密闭的容器中进行反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
| A. | 把铁块换成铁粉 | |
| B. | 将容器的体积压缩至原体积的一半 | |
| C. | 若保持压强不变,充入氮气使容器的体积增大 | |
| D. | 若保持体积不变,充入氮气使容器内的压强增大 |
8.反应2A(g)?2B(g)+C(g)△H>0,达平衡时,要使v(正)增大、c(A) 降低,应采取的措施是( )
| A. | 加压 | B. | 加催化剂 | C. | 降温 | D. | 升温 |
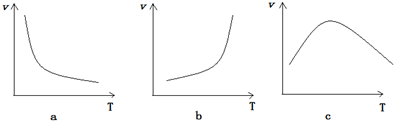
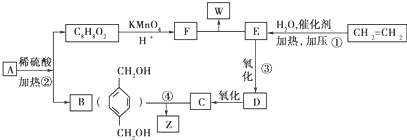
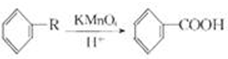 ,
,
 +2CH3COOH$→_{△}^{浓硫酸}$
+2CH3COOH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.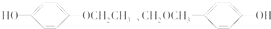 、
、 、
、 .
.