题目内容
【题目】室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2,且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是
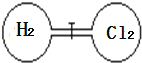
A. 开始时左右两室分子数相同
B. 最终容器内无H2存在
C. 反应前后H2室压强相同
D. 最终容器内密度与原来相同
【答案】D
【解析】试题分析:A、开始时左右两室中气体体积相同,气体密度相同,所以气体质量相同,但氢气和氯气摩尔质量不同,气体物质的量不同,分子数不同,故A错误;B、开始时左右两室中气体体积相同,气体密度相同,所以气体质量相同,氢气的物质的量大于氯气,反应后氢气过量,故B错误;C、氢气和氯气发生的反应为:H2+Cl2=2HCl;属于气体体积不变的反应,反应前氢气的压强大于氯气,反应后氢气室的压强减小,故C错误;D、化学反应遵循质量守恒定律,即反应前后质量不变,容器体积也不变,所以总密度不变,故D正确;故选D。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目