题目内容
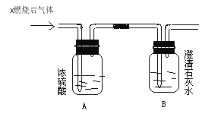
【题目】在实验室里用浓盐酸与高锰酸钾反应来制取少量的氯气,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.反应物中,氧化剂是;化合价升高的元素是 . 反应中HCl的作用是 .
【答案】KMnO4;Cl;酸性和还原性(或还原剂)
【解析】解:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价降低,则氧化剂为KMnO4 , Cl元素的化合价升高,该反应中生成两种盐体现盐酸的酸性、生成氯气时失去电子体现HCl的还原性,所以答案是:KMnO4;Cl;酸性和还原性(或还原剂).

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目