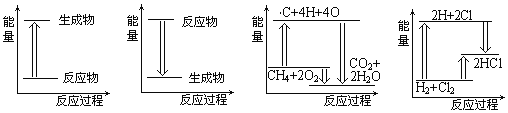
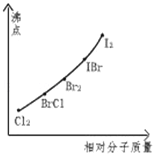
��Ŀ����
����Ŀ����6�֣�����ͼ��ʾ��װ��A�У���KMnO4�����Ũ��������ȡCl2����Ӧ�����ӷ���ʽΪ��2MnO4��+10Cl��+16H+=2Mn2++5Cl2��+8H2O��װ��B�е��Ĵ��������������´�������պ�е��ۡ�KI��Һ ��պ��Ʒ����Һ��պ����ɫʯ����Һ��պ��ŨNaOH��Һ����ͼ�мг�װ������ȥ����

�ش��������⣺
��1��p��ʢװ�Լ�������Ϊ ��
��2����Ӧ��ʼ�۲쵽��ʵ�������ǣ�
������ �������� ��
������ ��
��3��д��������Ӧ�����ӷ�ʽ�� ��
���𰸡���1����Һ©�� ��2�������� ���� ������ ��ɫ ������ �ȱ�����ɫ
��3�� Cl2+2OH��=Cl��+ClO����H2O
��������
�����������1��pװ��Ϊ��Һ©����2��������Cl2��2I��=I2��2Cl������ʹ��ֽ����ɫ������������ˮ�����˾���Ư���ԵĴ����Cl2��H2O=HCl��HClO����Ʒ�콫��ɫ������������ˮ���������ᣬʹ��ɫʯ����Һ��죬��Ѹ�ٽ���������Ư����ɫ��3�����������ж����������β�����գ�һ���ü�Һ��Cl2+2OH��=Cl��+ClO����H2O

 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�����Ŀ�������ʷ��������ȷ����
A | B | C | D | |
ǿ����� | HBr | FeCl3 | H3PO4 | Ca(OH)2 |
������� | HF | HCOOH | BaSO4 | HI |
�ǵ���� | CCl4 | Cu | H2O | C2H5OH |
A. A B. B C. C D. D
����Ŀ������������һ�ֹ�ҵ�Σ������ʳ�ηdz����ƣ����Խ�ǿ��
��.���飺��Ksp(AgNO2)=2��10��8��Ksp(AgCl)=1.8��10��10����Ka(HNO2)=5.1��10��4���������ķ�������NaNO2��NaCl���ֹ���______________________
��. ijС��ͬѧ������װ�ã���ȥ�г��������Ʊ���������
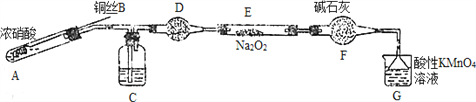
��֪����2NO��Na2O2=2NaNO2�� �����������£�NO��NO2������MnO4����Ӧ����NO3����Mn2����
��1��ʹ��ͭ˿���ŵ���________________________��
��2��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________________��
װ��C��ʢ�ŵ�ҩƷ��_________��������ĸ���ţ�
A��Ũ���� B��NaOH��Һ C��ˮ D�����Ȼ�̼
��3����С���ȡ5.000g��ȡ����Ʒ����ˮ���250ml��Һ��ȡ25.00ml��Һ����ƿ�У�
��0.1000mol��L��1����KMnO4��Һ���еζ���ʵ�������������±���ʾ��
����� | 1 | 2 | 3 | 4 |
����KMnO4��Һ���/mL | 20.90 | 20.12 | 20.00 | 19.88 |
�ٵ�һ��ʵ�����ݳ����쳣����������쳣��ԭ�������_________������ĸ���ţ���
a����ƿϴ����δ����
b����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ
c���ζ��յ�ʱ���Ӷ���
������KMnO4��Һ�ζ�����������Һ�����ӷ���ʽΪ___________________��
�۸���Ʒ���������Ƶ���������Ϊ______________��