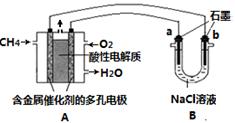
��Ŀ����
��1����һ���������İ�������������ܱ���������У���������������䣬��������������Բ��ƣ����ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺
H2NCOONH4��s�� 2NH3��g��+CO2��g��
2NH3��g��+CO2��g��
ʵ���ò�ͬ�¶��µ�ƽ�����������±���
| �¶ȣ��棩 | 15��0 | 20.0 | 25��0 | 30��0 | 35��0 |
| ƽ��������Ũ�ȣ���10��3 mol/L�� | 2��4 | 3��4 | 4��8 | 6.8 | 9��4 |
�ٰ�������立ֽⷴӦ���ʱ��H 0���>������<����=������
�ڿ����жϸ÷ֽⷴӦ�Ѿ��ﵽ��ѧƽ�����____��
A��2v��NH3��=v��CO2��
B���ܱ���������ѹǿ����
C���ܱ������л��������ܶȲ���
D���ܱ������а����������������
�۸��ݱ������ݣ�����25.0��ʱ�ķֽ�ƽ�ⳣ��Ϊ ��
��2��25��ʱ��NH3��H2O���볣��Kb=1��8��10��5��Mg��OH��2���ܶȻ�����Ksp=1��8��10��11����pH�Ʋ��0.5 mol/L��ˮ��Һ��pHԼΪ ����ij�Ȼ�þ��Һ�м���һ������ijŨ�ȵ��ռ��û��ҺpH =11��0������¶��²�������Һ�е�c��Mg2+��=____������֪lg2��0��3��lg3��0��5����
�� ��> (1��)��Bc(2��)��1.64��10-8mol3/L3 ����д��λ���۷֣���λд��0�֣�(2��)
��11.5(2��) 1.8��10-5mol/L(2��,��ֵ��ȷ��λ��1��)
����

��1��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� 2NH3��g�� ��H=��92.4 kJ/mol
2NH3��g�� ��H=��92.4 kJ/mol
���ڸ��¶�ʱ��ȡl mol N2��3 mol H2�����ܱ������У��ڴ��������½��з�Ӧ����÷�Ӧ�ų�����������_______92.4 kJ��(�С�ڡ��� �����ڡ� ���ڡ�)
��һ�������£��������淴Ӧ������̶����ܱ������н��У�����������˵����Ӧ�Ѵﵽƽ�����_______________��
| A��NH3���ɵ�������NH3�ֽ��������� |
B���������ķ�Ӧ���� v����NH3��=v����H2�� v����NH3��=v����H2�� |
| C�������ڵ��ܶȲ��ٱ仯 |
| D����λʱ��������a mol N2��ͬʱ����2a mol NH3 |
 ֵ��_____(����� ����С�� ���䡱)��
ֵ��_____(����� ����С�� ���䡱)����3�������£���0.001mol/LAlCl3��Һ��ͨ��NH3ֱ����������PH=_________ʱ����ʼ���ɳ���(��֪��Ksp[Al(OH)3]=1.0��10-33)
(14��)��ҵ���������Ҫ��Ӧ��4NH3(g)+5O2(g)  4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
(1)�����4molNH3��5molO2���������У��ﵽƽ��ʱ���ų�����0.8akJ����Ӧʱת�Ƶĵ�����Ϊ
mol
(2)�������������䣬���й�ϵͼ�д������ ��ѡ����ţ�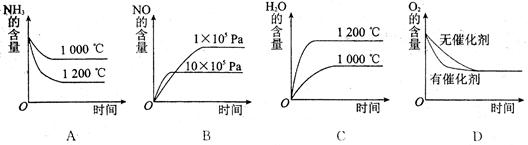
(3)t��ʱ�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�����±�
| Ũ��(mol/L) ʱ��(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| �� ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | x | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�ٷ�Ӧ�ڵ�2mim����4mimʱ����Ӧ����v(O2)=
�ڵ�2minʱ�ı����������ı������������
A�������¶� B��ʹ���˴��� C����Сѹǿ D��������������
������ͬ���¶��£���ʼ�������м���NH3��O2��NO��H2O(g)��Ũ�ȶ�Ϊ1mol/L����÷�Ӧ���� _______�������(�����Ӧ��.���淴Ӧ��.�����ƶ���)
��4����ҵ����ˮ���ն��������������ᣬ���ɵ�NO2���徭��������������յ�ѭ������ʹ����ת��Ϊ���ᣨ�ٶ�������������������ʧ��������23��NO2����2���������յõ�20�G��ϡ���� �֡�
��5����Ʒ�����Ũ��Ϊ60%��70%��Ϊ����Ũ���ᣬ����Mg(NO3)2����ˮ����Ȼ�����������CaCl2��MgCl2����ˮ����ԭ����__________________________________________
��2 L�ܱ������У�800 ��ʱ��Ӧ2NO(g)��O2(g)  2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
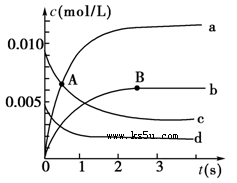
��1��A�㴦��v(��)________v(��)��A������Ӧ����________B������Ӧ����(�á����ڡ�����С�ڡ����ڡ����)��
��2����ͼ�б�ʾNO2�ı仯��������________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��________________��
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d�������ڵ��ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ�����������________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
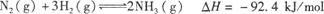 ���ݴ˻ش��������⣺
���ݴ˻ش��������⣺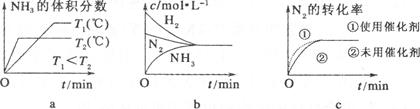
 2B(s) + 6HBr(g) ����ȡ���������������գ�
2B(s) + 6HBr(g) ����ȡ���������������գ�
 CH3OH(g)+H2O(g)����ͼ1��ʾ�÷�Ӧ����������(��λΪkJ��mol-1)�ı仯��
CH3OH(g)+H2O(g)����ͼ1��ʾ�÷�Ӧ����������(��λΪkJ��mol-1)�ı仯��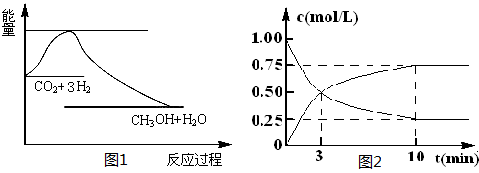
 2CO2(g)+ N2(g)�����ܱ�����
2CO2(g)+ N2(g)�����ܱ�����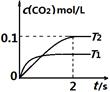
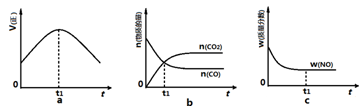
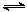 N2O4(g) ��H����56.9 kJ/mol ��
N2O4(g) ��H����56.9 kJ/mol ��