题目内容
【题目】已知,常温下,有氧化还原反应(未配平):HFeO4-+(NH2)2CS+H2O→Fe(OH)3+(NH2)2CO+SO42-+OH,下列有关说法正确的是
A. HFeO4-为还原剂,Fe(OH)3为氧化产物
B. 氧化剂与还原剂反应的物质的量之比为4∶3
C. 随着反应的进行,溶液中c(H+)/Kw逐渐变小
D. 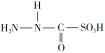 为此反应的中间产物,其中碳元素的化合价为0价
为此反应的中间产物,其中碳元素的化合价为0价
【答案】C
【解析】
A.Fe化合价由+6价降低到+3价,HFeO4-应该为氧化剂,Fe(OH)3为还原产物,故A错误;
B.HFeO4-为氧化剂,Fe化合价变化3,(NH2)2CS为还原剂,S化合价从2到+6变化8,氧化剂与还原剂反应的物质的量之比为8∶3,故B错误;
C.随着反应的进行,溶液中c(H+)逐渐变小,Kw不变,c(H+)/Kw逐渐变小,故C正确;
D.C与N相连C显正价,C与S相连C也显正价,C不可能为0价,故D错误;
故答案为C。

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目