题目内容
【题目】化合物F是合成降血脂药物阿伐他汀的重要中间体,其合成路线如下:

(1)化合物D中的含氧官能团为酰胺键、_____________和_____________(填官能团名称)。
(2)反应①→⑤中,属于取代反应的是_____________(填序号)。
(3)此合成路线中F的产率不高,原因是反应①中还有一种和B互为同分异构体的副产物生成,其结构简式为_____________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:_____________。
I.分子中含有一个含氧5元环;II.可使溴水褪色;
III.核磁共振氢谱显示氢原子的峰值比为1︰1︰2︰3。
(5)请以CH3COOC2H5和HCHO为原料制备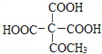 ,写出相应的合成路线流程图________(无机试剂任用,合成路线流程图示例见本题题干)。
,写出相应的合成路线流程图________(无机试剂任用,合成路线流程图示例见本题题干)。
【答案】 羟基 羰基 ①② ![]()
![]()

【解析】试题分析:
(1) 中的含氧官能团为酰胺键、羰基和羟基。
中的含氧官能团为酰胺键、羰基和羟基。
(2)根据流程图,反应①→⑤分别是取代反应、取代反应、加成反应、消去反应、加成反应。
(3)根据反应 ①的原理,![]() 可能还生成
可能还生成![]() ;
;
(4)可使溴水褪色,说明含有碳碳双键;核磁共振氢谱显示氢原子的峰值比为1︰1︰2︰3,说明结构对称,满足下列条件的B的一种同分异构体的结构简式。
(5)根据题目流程图,结合CH3COOC2H5的结构制备 。
。
解析:根据以上分析,(1) 中的含氧官能团为酰胺键、羰基和羟基。
中的含氧官能团为酰胺键、羰基和羟基。
(2)根据流程图,①→⑤分别是取代反应、取代反应、加成反应、消去反应、加成反应,属于取代反应的是①②。
(3)根据反应 ①的原理,![]() 可能还生成
可能还生成![]() ;
;
(4)分子中含有一个含氧5元环;可使溴水褪色,说明含有碳碳双键;核磁共振氢谱显示氢原子的峰值比为1︰1︰2︰3,说明结构对称,满足下列条件的B的同分异构体的结构简式为![]() 。
。
(5)根据题目流程图,结合CH3COOC2H5的结构制备 的流程图是
的流程图是 。
。








