题目内容
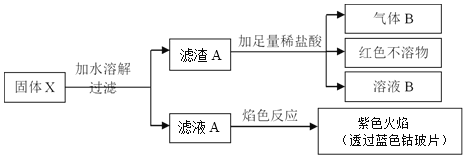
【题目】为了探究某固体化合物X(含三种元素)的组成和性质,设计并完成如下实验,其中气体C能使带火星的木条复燃。

请回答:
(1)白色沉淀D是_______。
(2)固体A中物质生成B和C的化学方程式为__________________。
(3)X的化学式是_________。
【答案】AgCl 2KClO3![]() 2KCl+3O2↑ KClO2
2KCl+3O2↑ KClO2
【解析】
由题干信息,气体C能使带火星的木条复燃,则气体C为O2,由于固体化合物X中含三种元素,根据转化关系及反应条件可知,31.95g固体A与MnO2反应得到固体B和标况下6.72L(0.3mol)O2,固体A中含有KClO3,物质的量为0.2mol,质量为24.5g,固体B为KCl,固体B溶解后加入过量的AgNO3溶液得到43.05g白色沉淀D,即AgCl的白色沉淀,则AgCl的物质的量为0.3mol,根据Cl原子守恒可知,B中KCl的物质的量为0.3mol,其中有0.2mol来自于KClO3的分解,另外0.1mol来自于31.95g固体化合物X隔绝空气加强热得到,则X→A可能为KClO2发生歧化反应生成KClO3和KCl,反应方程式为3KClO2![]() 2KClO3+KCl,即KClO2的物质的量为0.3mol,质量为31.95g,满足条件,据此分析解答问题。
2KClO3+KCl,即KClO2的物质的量为0.3mol,质量为31.95g,满足条件,据此分析解答问题。
(1)根据上述分析可知,白色沉淀D为AgCl;
(2)固体A中物质生成B和C为KClO3在MnO2作催化剂的条件下受热分解生成KCl和O2的反应,其化学方程式为2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)由上述分析可知,X→A为KClO2发生歧化反应生成KClO3和KCl,因此固体X为KClO2。

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目